Page 186 - 精细化工2019年第9期
P. 186
·1914· 精细化工 FINE CHEMICALS 第 36 卷
的条件下对不同染料的吸附性能比较。由图可知,
H 6 P 2 W 18 O 62 /MIL-101(Fe)对罗丹明 B、亚甲基蓝、孔
雀石绿的吸附效果很强,但对甲基橙的吸附效果不
佳。因为罗丹明 B、亚甲基蓝、孔雀石绿都属于阳
离子染料,甲基橙属于阴离子染料,H 6P 2W 18O 62/ MIL-
6–
101(Fe)在酸性条件下可电离出杂多阴离子[P 2 W 18 O 62 ] ,
根据离子间的静电作用,吸附剂对阳离子染料有很
强的选择性吸附。
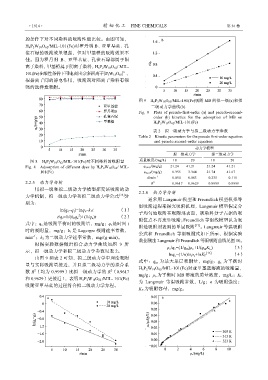
图 9 H 6 P 2 W 18 O 62 /MIL-101(Fe)吸附 MB 的拟一级(a)和拟
二级动力学曲线(b)
Fig. 9 Plots of pseudo-first-order (a) and pseudo-second-
order (b) kinetics for the adsorption of MB on
H 6 P 2 W 18 O 62 /MIL-101(Fe)
表 2 拟一级动力学与拟二级动力学参数
Table 2 Kinetic parameters for the pseudo first-order equation
and pseudo second-order equation
动力学模型
拟一级动力学 拟二级动力学
图 8 H 6 P 2 W 18 O 62 /MIL-101(Fe)对不同染料的吸附量 质量浓度/(mg/L) 10 20 10 20
Fig. 8 Adsorption of different dyes by H 6 P 2 W 18 O 62 / MIL- q e,exp/(mg/g) 21.24 41.21 21.24 41.21
101(Fe) q e,cal/(mg/g) 0.355 3.344 21.74 41.67
k/min 0.054 0.083 0.235 0.115
–1
2.2.5 动力学分析 R 2 0.9617 0.9629 0.9999 0.9999
用拟一级和拟二级动力学模型探究该吸附的动 2.2.6 热力学分析
力学机制,拟一级动力学和拟二级动力学公式 [16] 分
通常用 Langmuir 模型和 Freundlich 模型模拟等
别为:
温吸附过程来探究吸附机理,Langmuir 模型假定分
l n ( q e –q t )=lnq e –k 1 t (1) 子均匀地吸附在吸附剂表面,被染料分子占据的吸
2
t/q t =1/(k 2 q e )+(1/q e )t (2)
附位点不再发生吸附;Freundlich 等温线模型认为吸
式中:q e 是吸附平衡时的吸附量,mg/g;q t 是时间 t
附是吸附剂表面的单层吸附 [17] 。Langmuir 等温吸附
时的吸附量,mg/g;k 1 是 Lagergre 吸附速率常数, 公式和 Freundlich 等温吸附式如下所示,根据实验
–1
min ;k 2 为二级动力学速率常数,mg/(g·min)。
数据做出 Langmuir 和 Freundlich 等温吸附曲线见图 10。
根据实验数据做出拟合动力学曲线如图 9 所
ρ e /q e =(1/q m )ρ e +1/(q m K L ) (3)
示,拟一级动力学和拟二级动力学参数见表 2。
l n q e =(1/n)lnρ e +lnK F [16] (4)
由图 9 和表 2 可知,拟二级动力学中理论吸附
式中:q m 为最大单层吸附量,mg/g;q e 为平衡时
量与实际吸附量接近,并且拟二级动力学的拟合系 H 6 P 2 W 18 O 62 /MIL-101(Fe)对亚甲基蓝溶液的吸附量,
2
2
数 R (均为 0.9999)比拟一级动力学的 R (0.9617
mg/g;ρ e 为平衡时 MB 溶液的质量浓度,mg/L;K L
和 0.9629)更接近 1,表明 H 6P 2W 18O 62 /MIL- 101(Fe)
为 Langmuir 等温吸附常数,L/g;n 为吸附强度;
吸附亚甲基蓝的过程符合拟二级动力学方程。 K F 为吸附容量,mg/g。