Page 121 - 《精细化工》2020年 第10期
P. 121
第 10 期 谷雨桐,等: 铜基金属有机大环催化叠氮-炔烃环加成反应 ·2051·
应 2 h 后,产物 3a 的产率为 20.7%,反应 4 h 后, 表 3 光催化 CuAAC 的底物拓展
产率大大提高到 68.5%,6 h 收率为 88.5%,反应在 Table 3 Scope of the photocatalytic CuAAC
8 h 后基本完成,收率达到 94.3%,继续跟踪,10 h
收率为 98.0%,直到反应至 12 h,达到完全转化,
产率达到 100%。动力学曲线的前部具有明显的线性 产物编号 取代基 结构式 产率/%
增长趋势,而后部逐渐变平,这是非常明显的类酶
催化过程。 3a H 100.0
3b CH 3 81.3
3c OCH 3 82.6
3d Cl 99.0
3e CN 100.0
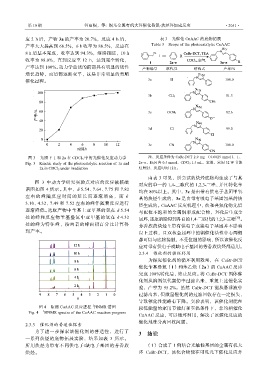
图 3 光照下 1 和 2a 在 CDCl 3 中的光催化反应动力学 注:反应条件为 CuBr-DCT 2.9 mg (0.0025 mmol),1、
Fig. 3 Kinetic study of the photocatalytic reaction of 1a and 2a~e、Et 3N 各 0.5 mmol,CDCl 3 1.5 mL,室温,家用 32 W 节能
2a in CDCl 3 under irradiation 灯照射,反应时间 12 h。
由表 3 可见,所尝试的炔烃底物均生成了与其
图 3 中动力学研究实验点对应的反应液核磁
对应的单一的 1,4-二取代的 1,2,3-三唑,并且转化率
谱图如图 4 所示。其中, δ5.54、7.64、7.75 和 7.82
均在 80%以上。其中,3c 是由带有供电子基团甲氧
左右的峰随反应时间的延长而逐渐增高,而δ
基的炔烃生成的,3e 是由带有吸电子基团氰基的炔
3.10、4.32、7.49 和 7.52 左右的峰伴随着反应进行 烃生成的。CuAAC 反应机理中,炔和叠氮化物先后
逐渐降低。选取产物中苄基上亚甲基的氢在δ5.54
与配位不饱和的金属铜形成配合物,环化后生成金
处的峰和反应物苄基叠氮中亚甲基的氢在δ4.32 属环,还原消除得到各自的1,4-二取代的1,2,3-三唑 [30] 。
处的峰为特征峰,按两者的峰面积百分比计算得 芳香族的炔烃上带有供电子或缺电子基团并不影响
到产率。 以上过程,且双核金属环中的铜催化活性中心两侧
都可以与底物接触,不受位阻的影响,所以该催化反
应对带有供电子或缺电子基团的芳香族炔烃都适用。
2.3.4 催化剂的循环利用
为探究催化剂的循环利用效果,在 CuBr-DCT
催化苄基叠氮(1)和苯乙炔(2a)的 CuAAC 反应
完成 100%转化后,终止反应。将 CuBr-DCT 固体催
化剂从溶剂氘代氯仿中过滤出来,重复上述催化实
验,产率为 95.2%。虽然 CuBr-DCT 能从悬浮液中
过滤出来,但微量催化剂的过滤回收存在一定损失,
导致催化性能略有下降。实验表明,该催化剂能在
1
图 4 监测 CuAAC 反应进程 HNMR 谱图 较低能量的家用节能灯和室温条件下,非均相催化
Fig. 4 HNMR spectra of the CuAAC reaction progress CuAAC 反应,可以循环利用,解决了该催化反应的
1
2.3.3 催化剂的普适性探索 催化剂难分离回收问题。
为了进一步探索该催化剂的普适性,进行了 3 结论
一系列炔烃的底物拓展实验,结果如表 3 所示。
所用炔烃为带有不同供电子/缺电子基团的芳香族 (1)合成了 1 例结合光敏性基团的金属有机大
炔烃。 环 CuBr-DCT,该化合物能在可见光下催化反应并