Page 195 - 《精细化工》2022年第8期
P. 195
第 8 期 曾敏静,等: 好氧颗粒污泥对钇离子的吸附-解吸性能 ·1695·
3+
升量约为 15%),并且吸附速率提升至与 0.6~1.0 mm 更准确表达 AGS 对 Y 吸附过程,表明化学吸附在
AGS 相当。可见,碾压破碎法是提升大粒径 AGS 吸附过程中起主导作用 [25] 。由图 3c 和表 3 可知,
3+
吸附能力的有效手段,推测原因可能为小粒径吸附 Webber-Morris 方程吸附常数 R 随着 Y 初始质量浓
剂具有更大的比表面积,因而具有更高吸附能力, 度增加而减小(表 3),说明颗粒内扩散是控制吸附
这与冉艳等 [24] 的研究结果一致。 速率的主要因素。
2.2 吸附动力学
在曝气混合、pH=4、不添加盐和其余重金属离 表 3 吸附动力学模型参数
Table 3 Parameters of adsorption kinetics models
子条件下进行动力学、热力学实验,结果见图 3。
/(mg/L) 25 50 100 拟合方程
0
Q e 5.9 11.7 19
伪一级 K 1 0.066 0.067 0.049 ln(Q e Q t ) lnQ e K t 1
R 2 0.58 0.74 0.6
5.84 11.72 19.27
Q e
t 1 1
伪二级 K 2 3.512 11.806 45.849 K 2 2 t
Q t Q e Q e
R 2 0.99 0.99 0.99
0.137 0.339 0.689
K 3
Webber- C 4.59 8.417 12.526 Q K t 1/2 C
Morris R 2 0.61 0.54 0.67 t 3
R 0.778 0.719 0.65
3+
注: 为 Y 初始质量浓度(mg/L);Q e 为平衡时的吸附量(mg/g
0
–1
MLSS);Q t 为 t 时刻的吸附量(mg/g MLSS);K 1 (min )、K 2 (mg·min/g
0.5
MLSS)、K 3 〔mg/(g MLSS·min )〕、C(mg/g MLSS)、R 均
为吸附常数。
2.3 吸附热力学
通过 Langmuir 和 Freundlich 方程对吸附结果进
行热力学拟合,结果见图 4。
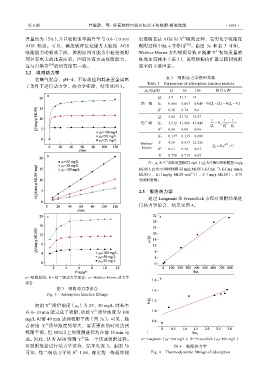
a—吸附曲线;b—伪二级动力学拟合;c—Webber-Morris 动力学
拟合
图 3 吸附动力学拟合
Fig. 3 Adsorption kinetics fittings
3+
初始 Y 质量浓度(ρ 0 )为 25、50 mg/L 时基本
3+
在 0~10 min 就完成了吸附,初始 Y 质量浓度为 100
mg/L 时需 40 min 达到吸附平衡(图 3a)。可见,随
3+
着初始 Y 质量浓度的增大,需要更长的时间达到
吸附平衡,但 80%以上的吸附进程均在前 10 min 完
3+
成。因此,认为 AGS 吸附 Y 是一个快速吸附过程。 a—Langmuir(ρ 0=100 mg/L);b—Freundlich(ρ 0=100 mg/L)
对吸附数据进行动力学拟合,结果见表 3。由图 3b 图 4 吸附热力学
2
可知,伪二级动力学的 R =1.00,相比伪一级模型能 Fig. 4 Thermodynamic fittings of adsorption