Page 78 - 精细化工2019年第10期
P. 78
·2044· 精细化工 FINE CHEMICALS 第 36 卷
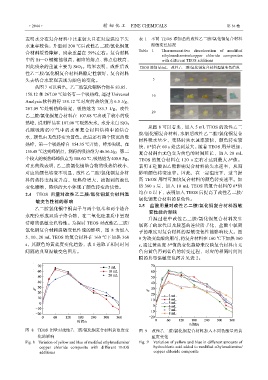
表明水分在复合材料中比重较大且在对应温度下失 表 1 不同 TEOS 添加量的改性乙二胺/氯化铜复合材料
水速率较快;升温到 200 ℃后改性乙二胺/氯化铜复 温敏变色情况
Table 1 Thermosensitive discoloration of modified
合材料缓慢降解,残余重量在 59%左右。复合材料
ethylenediamine/copper chloride composites
中的 Si—O 键键能很高,相应的熔点、沸点也较高, with different TEOS additions
因此残余的重量主要为 SiO 2 。结果表明,改性后改 TEOS 添加量/mL 改性乙二胺/氯化铜复合材料温敏变色情况
性乙二胺/氯化铜复合材料热稳定性较好,复合材料
失去结合水宏观表现为颜色的变化。 5
从图 7 可以看出,乙二胺氯化铜络合物在 83.85、
158.12 和 267.09 ℃处各有一个吸热峰,通过 Universal 10
Analysis 软件测得 158.12 ℃对应的热焓值为 6.5 J/g,
267.09 ℃处吸热峰较宽,吸热焓为 185.3 J/g。改性
20
乙二胺/氯化铜复合材料在 107.08 ℃出现了较小的吸
热峰,说明样品在 107.08 ℃吸热失水,水分来自 SiO 2
从图 8 可以看出,加入 5 mL TEOS 的改性乙二
孔隙吸附的空气中的水和复合材料结构中的结合
胺/氯化铜复合材料,水解后改性乙二胺/氯化铜复合
水,颜色由无色转变为黄色。此后还有两个较宽的吸
材料吸水量少,受热时失水速率较快,颜色转变较
热峰,第一个吸热峰自 154.35 ℃开始,峰形尖锐,在
快,b*值在 60 s 处达到最大。随着 TEOS 用量增加,
155.48 ℃达到峰值点,测得的吸热焓为 46.56 J/g;第二 复合材料由无色变为黄色的时间延长,加入 20 mL
个较大的吸热峰峰值点为188.60 ℃,吸热焓为400.0 J/g。 TEOS 的复合材料在 120 s 左右才达到最大 b*值。
对比曲线表明,乙二胺氯化铜络合物的吸热焓较小, 表明正硅酸四乙酯影响复合材料的失水速率,从而
对应的颜色转变不明显,改性乙二胺/氯化铜复合材 影响颜色转变速率。因此,在一定温度下,适当提
料的热转变温度升高,吸热焓增大,捕捉到的颜色 高 TEOS 用量可加快复合材料的颜色转变速率。加
变化清晰,热焓的大小体现了颜色转变的快慢。 热 360 s 后,加入 10 mL TEOS 的复合材料的 b*值
2.4 TEOS 用量对改性乙二胺/氯化铜复合材料温 均在 0 以下,表明加入 TEOS 后提高了改性乙二胺/
氯化铜复合材料的显色性。
敏变色性能的影响
2.5 盐酸用量对改性乙二胺/氯化铜复合材料温敏
乙二胺氯化铜中铜离子与两个氨基和两个结合
变性能的影响
水配位形成双质子络合物,在二氧化硅基质中呈现
升温过程中改性乙二胺/氯化铜复合材料发生
清晰的温敏变色特性。为探讨 TEOS 对改性乙二胺/
氯离子的取代以及胺基的连续质子化,盐酸中氯离
氯化铜复合材料温敏变色性能的影响,图 8 为加入 子的浓度对复合材料的温敏变色性能影响较大。图
5、10、20 mL TEOS 的复合材料在 160 ℃下加热 360 9 为改变盐酸的用量,将复合材料在 160 ℃下加热 360
s,其颜色的黄蓝度变化趋势,表 1 选取了相同时间 s,通过黄蓝度 b*值的变化趋势来反映复合材料由无
间隔的典型温敏变色图片。 色向黄色再到蓝色的转变过程,对应的相同时间间
隔的典型温敏变色图片见表 2。
图 8 TEOS 用量对改性乙二胺/氯化铜复合材料黄蓝度变 图 9 改性乙二胺/氯化铜复合材料加入不同盐酸量的黄
化的影响 蓝度变化
Fig. 8 Variation of yellow and blue of modified ethylenediamine/ Fig. 9 Variation of yellow and blue in different amounts of
copper chloride composite with different TEOS hydrochloric acid added to modified ethylenediamine/
additions copper chloride composite