Page 169 - 《精细化工》2020年第3期
P. 169
3+
3+
3+
第 3 期 章昌华,等: PAMAM 接枝稻草对 Nd 、Sm 、La 的吸附特性 ·587·
因在于 PAMAM 接枝稻草对稀土离子的吸附机理主 K
lg Q Q lgQ 1 t (2)
要是由于 PAMAM 的氨基官能团和稀土金属离子发 e t e 2.303
生配位作用 [12] 。吸附刚开始发生时,由于吸附剂表 t 1 t
(3)
面的氨基官能团数量众多,所以单位时间内能够和 Q t KQ e 2 Q e
2
大量的稀土金属离子发生配位作用,进而产生吸附 1 2
i
t
作用。而随着吸附时间的延长,吸附剂表面的氨基 Q K t C (4)
式中: Q 为平衡吸附量,mg/g; Q 为瞬时吸附量,
官能团数量越来越少,而且吸附在吸附剂表面的稀 e t
−1
土金属离子会和溶液主体中的稀土金属离子产生排 mg/g; K 为拟一级速率常数,h ; K 为拟二级速
2
1
斥作用,再加上空间位阻效应,这些因素的叠加导 率常数,g/(mg·h); K 为颗粒内扩散速率常数,
i
0.5
致吸附量增加趋缓,直至达到吸附平衡。 mg/(g·h )。
为了更好地理解吸附剂对溶液中客体小分子的 采用以上 3 种动力学方程来研究 4.0 代 PAMAM
3+
3+
3+
吸附动力学机理,研究者们提出了多种吸附动力学 接枝稻草吸附剂对 La 、Nd 、Sm 稀土金属离子
模型方程,其中应用最为广泛的有 Lagergren’s 拟一 吸附动力学过程,拟合得到的相关系数、平衡吸附
级〔式(2)〕、Ho’s 拟二级〔式(3)〕和内扩散模型方 量和动力学速率常数等数值见表 1。图 6 是拟二级
程〔式(4)〕 [13] 。 动力学方程的拟合曲线。
表 1 吸附动力学参数
Table 1 Kinetics parameters for the adsorption
Pseudo first order Pseudo second order Intraparticle diffusion
Q e-exp/(mg/g)
Q e-cal/(mg/g) K 1/h R 1 Q e-cal/(mg/g) K 2/〔g/(mg·h)〕 R 2 K i/〔mg/(g·h )〕 R 3 2
0.5
2
–1
2
3+
La 50.12 34.54 0.67 0.9581 58.04 0.02 0.9987 16.50 0.9427
Nb 47.14 38.33 0.69 0.9514 55.99 0.02 0.9980 16.60 0.9570
3+
3+
Sm 40.11 32.00 0.65 0.9439 49.38 0.02 0.9961 15.45 0.9504
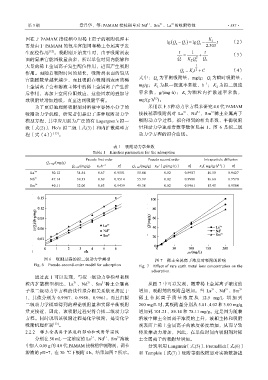
图 6 吸附过程的拟二级动力学模型 图 7 稀土金属离子浓度对吸附的影响
Fig. 6 Pseudo-second-order model for adsorption Fig. 7 Effect of rare earth metal ions concentration on the
adsorption
通过表 1 可以发现,与拟一级动力学模型和颗
3+
3+
3+
粒内扩散模型相比,La 、Nd 、Sm 稀土金属离 从图 7 中可以发现,随着稀土金属离子浓度的
3+
3+
子拟二级动力学方程的线性拟合相关系数更接近于 增加,吸附剂的吸附量增加。当 La 、Nd 、Sm 3+
1,其值分别为 0.9987、0.9980、0.9961。而且由拟 稀土金属 离子质量 浓度从 12.5 mg/L 增加 到
二级动力学模型得到的理论吸附量和实际平衡吸附 200 mg/L 时,其吸附量分别从 5.01、4.02 和 3.00 mg/g
量更接近,因此,该吸附过程更符合拟二级动力学 增加到 101.21、89.14 和 78.11 mg/g。这是因为随着
方程。同时说明该吸附过程是化学吸附,是受化学 溶液中稀土金属离子浓度的上升,液相主体和吸附
吸附机理控制 [13] 。 剂表面上稀土金属离子的浓度梯度增加,从而导致
2.2.2 稀土金属离子浓度的影响和吸附等温线 传质推动力增加,因此,在单位时间内吸附剂对稀
3+
3+
3+
分别在 50 mL 一定浓度的 La 、Nd 、Sm 溶液 土金属离子的吸附量增加。
中加入 0.05 g 的 4.0 代 PAMAM 接枝稻草吸附剂,调节 分别利用 Langmuir〔式(5)〕、Freundlich〔式(6)〕
溶液的 pH=7,在 30 ℃下吸附 4 h,结果如图 7 所示。 和 Tempkin〔式(7)〕吸附等温线模型对实验数据进