Page 222 - 《精细化工》2020年第2期
P. 222
·424· 精细化工 FINE CHEMICALS 第 38 卷
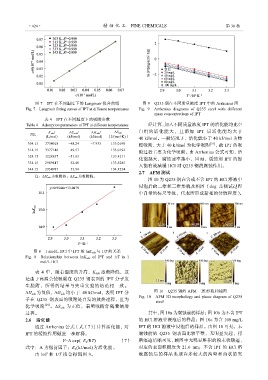
图 7 IPT 在不同温度下的 Langmuir 拟合曲线 图 9 Q235 钢在不同质量浓度 IPT 中的 Arrhenius 图
Fig. 7 Langmuir fitting curves of IPT at different temperatures Fig. 9 Arrhenius diagrams of Q235 steel with different
mass concentrations of IPT
表 4 IPT 在不同温度下的吸附参数
Table 4 Adsorption parameters of IPT at different temperatures 经计算,加入不同质量浓度 IPT 的活化能均比空
K ads/ ΔG ads/ ΔH ads/ ΔS ads 白组的活化能大,且添加 IPT 后活化能均大于
T/K
(L/mol) (kJ/mol) (kJ/mol) 〔J/(mol·K)〕
40 kJ/mol。一般情况下,活化能小于 40 kJ/mol 为物
304.15 3734018 –48.24 –7.935 133.0198 理吸附,大于 40 kJ/mol 为化学吸附 [21] ,故 IPT 的吸
314.15 3377146 –49.57 133.0192
附过程主要为化学吸附。由 Arrhenius 公式可知,活
324.15 3228837 –51.03 133.4211
化能越大,腐蚀速率越小,因而,缓蚀剂 IPT 的加
334.15 2989447 –52.40 133.5285
入能有效减缓 HCl 对 Q235 钢的腐蚀作用。
344.15 2954987 –53.94 134.1254
2.7 AFM 测试
注:ΔH ads 为吸附热;ΔS ads 为吸附熵。
图 10 为 Q235 钢在含或不含 IPT 的 HCl 溶液中
浸泡后的二维和三维形貌及相图(deg 是测试过程
中自带的标尺等级,代表所形成新相的分散程度)。
图 8 1 mol/L HCl 中 IPT 的 lnK ads 与 1/T 的关系
Fig. 8 Relationship between lnK ads of IPT and 1/T in 1
mol/L HCl
表 4 中,随着温度的升高,K ads 逐渐降低,这
是由于高温会使吸附在 Q235 钢表面的 IPT 分子发
生脱附,所得的结果与失重实验的结论相一致。
ΔH ads 为负值,ΔG ads 均小于–40 kJ/mol,表明 IPT 分 图 10 Q235 钢的 AFM 三维形貌和相图
Fig. 10 AFM 3D morphology and phase diagram of Q235
子在 Q235 钢表面的吸附是自发的放热过程,且为 steel
化学吸附 [20] 。ΔS ads 为正值,表明吸附伴随着熵增
过程。 其中,图 10a 为腐蚀前的样品;图 10b 为不含 IPT
2.6 活化能 的 HCl 溶液中浸泡后的样品;图 10c 为含 100 mg/L
通过 Arrhenius 公式〔式(7)〕计算活化能,对 IPT 的 HCl 溶液中浸泡后的样品。由图 10 可见,未
IPT 的缓蚀作用做进一步解释。 腐蚀前的 Q235 钢表面比较平整,无明显突起,打
V=A exp(–E a /RT) (7) 磨痕迹清晰可见,相图中无明显堆积的粉末状锈迹,
式中:A 为指前因子;E a (kJ/mol)为活化能。 对应的表面粗糙度为 21.6 nm;不含 IPT 的 HCl 溶
由 lnV 和 1/T 拟合得到图 9。 液腐蚀后的样品出现许多较大的沟壑和山状的突