Page 212 - 《精细化工)》2023年第10期
P. 212
·2290· 精细化工 FINE CHEMICALS 第 40 卷
C2、C3 和 C4 可酸溶态 Cu(Ⅱ)含量分别降低 6.01%、 和 20.07%,大于单独使用 OBs 和 OBDCs,较高毒
11.61%、13.50%、18.21%,C1、C2、C3 和 C4 可酸 性的可酸溶态向毒性较低的残渣态等形态转变。由
溶态 Pb 含量分别降低 5.87%、13.76%、16.58%、 于钝化剂表面官能团与黏土矿物的离子交换等作用
20.07%。可酸溶态金属向可还原态、可氧化态和残 使重金属离子迁移能力减弱,导致可浸出 Cu(Ⅱ)
渣态转变,使土壤中 Cu(Ⅱ)和 Pb(Ⅱ)的存在 和 Pb(Ⅱ)的量减少 [6] ,毒性降低,由于 OBDCs-OB
相对稳定。可酸溶态的 Pb(Ⅱ)占比远小于 Cu(Ⅱ), 加入后 Pb(Ⅱ)的可酸溶态含量远低于 Cu(Ⅱ),
说明对 Pb(Ⅱ)的钝化效果更好。该现象可以通过 所以 Pb(Ⅱ)的潜在浸出毒性远低于 Cu(Ⅱ)。
软硬酸碱理论来解释,硬酸(软酸)优先与硬碱(软
碱)结合,Pb(Ⅱ)为硬酸,与土壤中—OH(硬碱)
2+
等的络合度高于 Cu (软酸),这与相关报道结果相
−
似 [16] 。土壤 pH 较高时土壤环境出现 OH 等游离阴离
子,可与重金属离子形成沉淀 [28-29] 。黏土矿物层状结
构中的 Na(Ⅰ)、K(Ⅰ)等会与 Cu(Ⅱ)和 Pb(Ⅱ)
发生离子交换,从而起到钝化作用。
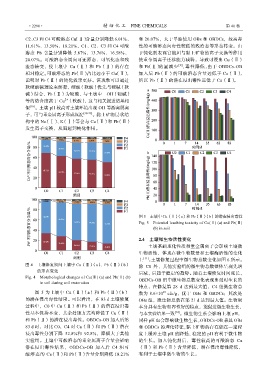
图 5 土壤中 Cu(Ⅱ)(a)和 Pb(Ⅱ)(b)的潜在浸出毒性
Fig. 5 Potential leaching toxicity of Cu(Ⅱ) (a) and Pb(Ⅱ)
(b) in soil
2.4 土壤微生物活性变化
土壤基础理化性质和重金属离子会影响土壤微
生物活性,体现在微生物数量和土壤酶活性的变化
上 [11] 。土壤修复过程中微生物总数变化如图 6 所示。
图 4 土壤修复期间土壤中 Cu(Ⅱ)(a)、Pb(Ⅱ)(b) 除 C0 外,其他实验组的微生物总数整体呈现先增
的形态变化
后减,后趋于稳定的趋势。随着土壤修复时间延长,
Fig. 4 Morphological changes of Cu(Ⅱ) (a) and Pb(Ⅱ) (b) OBDCs-OB 组中微生物总数变化表现出延时生长的
in soil during soil restoration
特点,在修复第 28 d 达到最大值,C4 组微生物总
图 5 为土壤中 Cu(Ⅱ)(a)和 Pb(Ⅱ)(b) 数为 8.6×10 10 cfu/g,优于 OBs 和 OBDCs;其次是
的潜在浸出毒性结果。可以看出,在 83 d 土壤修复 OBs 组,微生物总数在第 21 d 达到最大值。生物炭
过程中,C0 中 Cu(Ⅱ)和 Pb(Ⅱ)的潜在浸出毒 本身具有生物相容性好的特点,能促进微生物生长,
性基本保持不变,其余处理方式均降低了 Cu(Ⅱ) 与本实验结果一致 [14] 。微生物生长会影响土壤 pH,
和 Pb(Ⅱ)的潜在浸出毒性。OBDCs-OB 加入后第 同样 pH 也会影响微生物生长,OBDCs-OB 兼具 OBs
83 d 时,对比 C0,C4 对 Cu(Ⅱ)和 Pb(Ⅱ)潜在 和 OBDCs 的理化特征,黏土矿物的存在能在一定程
浸出毒性分别下降 52.8%和 92.8%,降幅大于其他 度上缓冲土壤 pH 的降低,稳定的 pH 有利于微生物
实验组。土壤中可酸溶态的重金属离子含量会影响 的生长。加入钝化剂后,毒性较高的可酸溶态 Cu
潜在浸出毒性结果,OBDCs-OB 加入后 C4 组可 (Ⅱ)和 Pb(Ⅱ)含量降低,潜在浸出毒性降低,
酸溶态的 Cu(Ⅱ)和 Pb(Ⅱ)含量分别降低 18.21% 有利于土壤中微生物的生长。