Page 172 - 精细化工2019年第10期
P. 172
·2138· 精细化工 FINE CHEMICALS 第 36 卷
氧化 n 分钟后硫化物 a 的脱除率(η an )和总脱
除率(η Tn )计算公式如(2)、(3)所示。
m m
an /% a0 an 100 (2)
m a0
m m 32
Tn /% a0 an 100 (3)
m a0 M a
式中:m a0 —油样 S 0 中硫化物 a 的质量,mg;M a —
硫化物 a 的相对分子质量,g/mol。
1.4 模型硫化物氧化产物分析
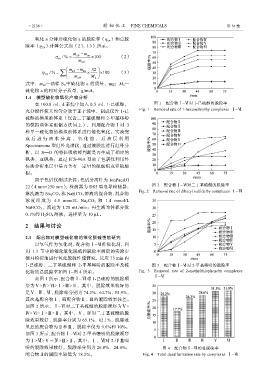
在 100.0 mL 正辛烷中加入 0.5 mL 1-己硫醇, 图 1 配合物Ⅰ~Ⅵ对 1-己硫醇的脱除率
充分搅拌使其均匀分散于正辛烷中,制成仅含 1-己 Fig. 1 Removal rate of 1-hexanethiolby complexes Ⅰ~Ⅵ
硫醇的模拟油体系(仅含二丁基硫醚和 2-甲基噻吩
的模拟油体系配制方法同上),利用配合物Ⅰ对 3
种单一硫化物的模拟油体系进行催化氧化。实验完
成 后进行油 水分离, 氧化前、 后油层利 用
Spectrumone 型红外光谱仪,通过液膜法进行红外分
析,以 S==O 的特征吸收峰判断是否生成了相应的
砜类、亚砜类;通过 ICS-90A 型离子色谱仪利用外
标法分析水层中是否含有一定量的硫酸根或亚硫酸
根。
离子色谱仪测试条件:色谱分离柱为 IonPacAG
22(4 mm×250 mm);检测器为 DS5 型电导检测器; 图 2 配合物Ⅰ~Ⅵ对二丁基硫醚的脱除率
Fig. 2 Removal rate of dibutyl sulfide by complexes Ⅰ~Ⅵ
淋洗液为 Na 2 CO 3 和 NaHCO 3 溶液的混合物,混合物
浓度组成为 4.5 mmol/L Na 2 CO 3 和 1.4 mmol/L
NaHCO 3 ,流速为 1.20 mL/min;再生液为体积分数
0.1%的 H 2 SO 4 溶液;进样量为 10 μL。
2 结果与讨论
2.1 配合物对模型硫化物的催化脱硫性能研究
以氧气作为氧化剂,配合物Ⅰ~Ⅵ作催化剂,利
用 1.3 节中的催化氧化脱硫和脱除率测定的实验步
骤对模拟油进行氧化脱硫性能研究,反应 75 min 内
1-己硫醇、二丁基硫醚和 2-甲基噻吩的脱除率及硫 图 3 配合物Ⅰ~Ⅵ对 2-甲基噻吩的脱除率
化物的总脱除率如图 1~图 4 所示。 Fig. 3 Removal rate of 2-methylthiopheneby complexes
Ⅰ~Ⅵ
如图 1 所示,配合物Ⅰ~Ⅵ对 1-己硫醇的脱除顺
序为Ⅴ>Ⅳ>Ⅵ>Ⅰ>Ⅲ>Ⅱ,其中,脱除效果较好的
是Ⅴ、Ⅳ、Ⅵ,脱除率分别为 74.2%、64.7%、55.9%,
其次是配合物Ⅰ,而配合物Ⅱ、Ⅲ的脱除效果较差。
如图 2 所示,Ⅰ~Ⅵ对二丁基硫醚的脱除顺序为Ⅴ>
Ⅳ>Ⅵ>Ⅰ>Ⅲ>Ⅱ。其中,Ⅴ、Ⅳ对二丁基硫醚的脱
除效果较好,脱除率分别为 65.1%、62.1%,脱除效
果差的配合物为Ⅱ和Ⅲ,脱除率仅为 9.6%和 10%。
如图 3 所示,配合物Ⅰ~Ⅵ对 2-甲基噻吩的脱除顺序
为Ⅰ>Ⅵ>Ⅴ≈Ⅳ>Ⅲ>Ⅱ。其中,Ⅰ、Ⅵ对 2-甲基噻
吩的脱除效果较好,脱除率分别为 26.8%、24.4%; 图 4 配合物Ⅰ~Ⅵ的总脱硫率
配合物Ⅱ的脱除率较低为 18.2%。 Fig. 4 Total desulfurization rate by complexes Ⅰ~Ⅵ