Page 86 - 201904
P. 86
·612· 精细化工 FINE CHEMICALS 第 36 卷
与 PDA 相比,PDA/α-FeOOH 复合材料中既存 色由蓝色变为灰蓝色,其吸收光强度增加,650、595 nm
在 PDA 中—COOH 间的氢键作用,又存在 α-FeOOH 的吸收峰均有偏移(图 5b,PFe-6 水溶液混浊未提
+
表面—OH 与—COOH 之间的氢键作用以及—OH 2 供吸收光谱)。加热 PDA/α-FeOOH 复合材料,刺激
–
与—COO 间的静电作用,两种作用力影响了聚合物 了聚合物分子链的运动,原有的构象被破坏,形成
内各种片段的热运动,导致 PDA/α-FeOOH 复合材 新构象,复合材料由蓝色变为红色。受复合材料中
料加热至 70 ℃才转变为红色。当温度下降时,这两 α-FeOOH 含量影响,变色温度不一致,其中,PFe-3
种作用力促使聚合物分子链恢复至最初的排列, 复合材料随着加热温度的升高,波长位于 650、595
PDA/α-FeOOH 复合材料颜色又由红色变为蓝色,出 nm 的吸收光强度迅速下降,蓝色稳定的构象向红色
现“蓝红蓝”的可逆现象。 稳定的构象转变,最大吸收波长蓝移至 540 nm(图
2.2.2 α-FeOOH 用量对 PDA/α-FeOOH 复合材料热 5c),45 ℃已变红,60 ℃完全变为红色,比 PFe-1、
致变色温度的影响 PFe-2 提前 5~10 ℃。当二炔酸单体与 α-FeOOH 的质
将光照聚合 10 min 的 6 个 PDA/α-FeOOH 复合 量比≥2∶1,热致变色转换温度滞后,为 65 或 70 ℃
材料,即 PFe-1、PFe-2、PFe-3、PFe-4、PFe-5、PFe-6
完全变为红色。
加热,颜色变化如图 5a 所示。未加热的 PDA/ 2.2.3 不同光聚合时间对复合材料热致变色可逆的
α-FeOOH 复合材料随着 α-FeOOH 含量的增加,颜 影响
通常,聚二炔酸加热变色与其分子链构象变化
有关,引起构象变化的主要原因是聚合物分子链的
共轭长度,而聚合时间对分子链的共轭长度影响较
大。不同光聚合时间下 PFe-2 复合材料的紫外-可见
吸收谱图如图 6 所示,不同聚合时间制备的 PFe-2
复合材料的颜色不同,但最大吸收波长均位于 650 nm
左右,且 595 nm 附近出现了表明聚二炔酸共轭链长
短的肩峰 [27] 。光照≤15 min,最大吸收峰与肩峰的
吸光强度缓慢增加,表明复合材料中聚合物分子量
增大,其分子链的共轭长度变宽;光照15 min,最
大吸收峰吸收强度先增后降,而 595 nm 处的肩峰强
度持续增高,进一步说明聚二炔酸分子链中的共轭
长度随着光照时间的延长而增长 [27] 。
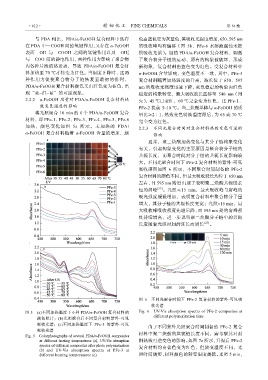
图 6 不同光聚合时间下 PFe-2 复合材料的紫外-可见吸
收光谱
图 5 (a)不同加热温度下 6 种 PDA/α-FeOOH 复合材料的 Fig. 6 UV-Vis absorption spectra of PFe-2 composites at
颜色照片;(b)光照聚合后不同复合材料紫外-可见 different polymerization time
吸收光谱;(c)不同加热温度下 PFe-3 的紫外-可见 由于不同紫外光照聚合时间制备的 PFe-2 复合
吸收光谱
Fig. 5 Colorphotographs of several PDA/α-FeOOH composites 材料中聚二炔酸的共轭链长度不同,需考察其对材
at different heating temperatures (a), UV-Vis absorption 料热致可逆变色的影响。如图 7a 所示,升温后 PFe-2
spectra of different composites after photo polymerization 复合材料均由蓝色变为红色,但转变温度不同,光
(b) and UV-Vis absorption spectra of PFe-3 at
different heating temperatures (c) 照时间越短,材料颜色的转变温度越低。光照 5 min,