Page 166 - 精细化工2019年第8期
P. 166
·1654· 精细化工 FINE CHEMICALS 第 36 卷
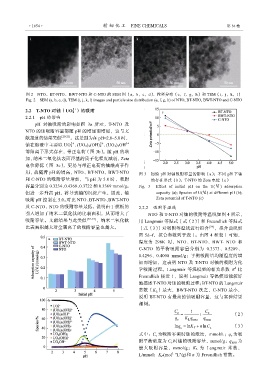
图 2 NTO、BT-NTO、BWT-NTO 和 C-NTO 的 SEM 图(a,b,c,d)、粒径分布(e,f,g,h)和 TEM(i,j,k,l)
Fig. 2 SEM (a, b, c, d), TEM (i, j, k, l) images and particle size distribution (e, f, g, h) of NTO, BT-NTO, BWT-NTO and C-NTO
2+
2.2 T-NTO 对铀(UO 2 )的吸附
2.2.1 pH 的影响
pH 对铀吸附的影响如图 3a 所示,T-NTO 及
NTO 的铀吸附容量都随 pH 的增加而增加,这与文
献报道的结果类似 [20-21] 。这是因为在 pH=2.0~5.0 时,
2+
2+
铀在溶液中主要以 UO 2 、(UO 2 ) 2 (OH) 2 、(UO 2 ) 3 OH 5+
等阳离子形式存在,带正电荷(图 3b)。随 pH 的增
加,纳米二氧化钛表面羟基的质子化程度减弱,Zeta
电位降低(图 3c),更易与带正电荷的铀酰离子作
用,故随着 pH 的增高,NTO、BT-NTO、BWT-NTO 图 3 初始 pH 对铀吸附容量的影响(a);不同 pH 下铀
和 C-NTO 的吸附容量增加,当 pH 为 5.0 时,吸附 的存在形式(b);T-NTO 的 Zeta 电位(c)
容量分别为 0.3234、0.4369、0.3722 和 0.3369 mmol/g。 Fig. 3 Effect of initial pH on the U( Ⅵ ) adsorption
但进一步升高 pH,将导致铀的沉淀产生,因此,铀 capacity (a); Species of U(Ⅵ) at different pH (b);
吸附 pH 控制在 5.0。对比 NTO、BT-NTO、BWT-NTO Zeta potential of T-NTO (c)
及 C-NTO,NTO 的吸附容量最低,说明由于模板的 2.2.2 吸附等温线
引入增加了纳米二氧化钛的比表面积,从而增大了 NTO 和 T-NTO 对铀的吸附等温线如图 4 所示,
吸附容量。文献结果与此类似 [22-23] ,纳米二氧化钛 用 Langmuir 等温式〔式(2)〕和 Freundlich 等温式
比表面积越大对金属离子的吸附容量也越大。 〔式(3)〕对吸附等温线进行拟合 [24] ,拟合曲线如
图 5d~f,拟合参数列于表 1。由图 4 和表 1 可知,
温度为 298K 时,NTO、BT-NTO、BWT- NTO 和
C-NTO 的平衡吸附容量分别为 0.3373、0.5209、
0.4296、0.4000 mmol/g;平衡吸附量均随温度的增
加而增加,这表明 NTO 及 T-NTO 对铀的吸附为化
2
学吸附过程。Langmuir 等温模型的相关系数 R 比
Freundlich 接近 1,说明 Langmuir 等温模型能较好
地描述 T-NTO 对铀的吸附过程;BT-NTO 的 Langmuir
常数(K L )最大,BWT-NTO 次之,C-NTO 最小,
说明 BT-NTO 有最高的铀吸附容量,这与实验结果
相同。
C e 1 C e (2)
q K q q
e L m a x m a x
lnq lnK n lnC (3)
e F e
式中:C e 为吸附平衡时铀的浓度,mmol/L;q e 为吸
附平衡浓度为 C e 时铀的吸附容量,mmol/g;q max 为
最大吸附容量,mmol/g;K L 为 Langmuir 常数,
L /g)和 n 为 Freundlich 常数。
L/mmol;K F (mol 1–n n