Page 96 - 《精细化工》2020年第4期
P. 96
·730· 精细化工 FINE CHEMICALS 第 37 卷
2.2 凝胶吸水性能测定 由图 3 可知,在 pH 相同的条件下,两种水凝
2.2.1 凝胶在不同温度、pH 溶液中溶胀性能 胶在 25 ℃下溶胀性能相似,随着环境温度升高,
以不同交联剂制备的水凝胶在不同温度、不同 以 TAAB 为交联剂制备的凝胶在 75 及 125 ℃均保
pH 水溶液中的溶胀性能如图 3 所示。其中,图 3a 持了优异的耐水解(保水)性能,溶胀倍率与常温
以 TAAB 为交联剂,图 3b 中所用凝胶是以市售通用 下相比变化不大;以 NMBA 为交联剂制备的凝胶在
交联剂 NMBA 制备。 75 ℃部分水解,125 ℃完全水解。这主要是 TAAB
与 NMBA 化学结构不同所致,通用交联剂 NMBA
形成的交联键中含有酰胺键,酰胺键高温易水解,
凝胶网络结构被破坏,耐水解性能较差,TAAB 中
形成的交联化学键中不含易水解化学键,因此在高
温环境中,以 TAAB 为交联剂所制凝胶吸水后的网
络结构几乎不受影响,表现出优异的耐水解性能。
在 pH=7、125 ℃下,P(AA-AMPS)/SA 在水溶液中
的吸水倍率可达 350.4 g/g。
不同 pH 条件下凝胶结构变化机理如图 4 所示。
在温度相同的条件下,水凝胶在不同 pH 水溶液中
溶胀性能相差较大。在强酸性(pH=2)和强碱性
(pH=12)环境中吸水倍率明显低于中性环境。如
+ – –
图 4 所示,在强酸性条件下,H 与—COO 、—SO 3
结合转变成—COOH、—SO 3 H,减小了凝胶内部的
电荷斥力,且—COOH、—SO 3 H 基团间还可以形
成氢键,凝胶网络内部自由空间骤然缩小,吸水倍
率降低;随着 pH 的增加,凝胶主链上的—COOH、
—SO 3 H 主要以离子形式存在,凝胶网络链间相互排
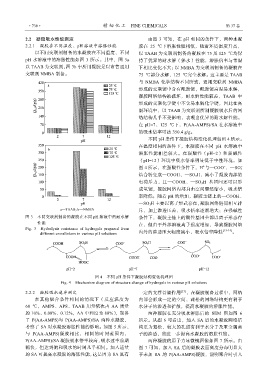
a—TAAB; b—NMBA 斥,加上渗透压差,吸水倍率逐渐增大;在强碱性
图 3 不同交联剂制备的凝胶在不同 pH 溶液中的耐水解 条件下,凝胶主链上的酸性基团全部以离子形态存
性能 在,但由于外部溶液离子强度增加,导致凝胶网络
Fig. 3 Hydrolysis resistance of hydrogels prepared from [13-14]
different crosslinkers in various pH solutions 内外的渗透压大幅度减小,吸水倍率降低 。
图 4 不同 pH 条件下凝胶结构变化机理图
Fig. 4 Mechanism diagram of structure change of hydrogels in various pH solutions
2.2.2 凝胶吸水速率测定 一定的支撑骨架作用 [15] ,在凝胶制备过程中,网络
在其他聚合条件相同的情况下(反应温度为 内部会形成一定的空间,疏松的网络结构更有利于
60 ℃,AMPS、APS、TAAB 用量依次占 AA 质量 水分子的渗透和扩散,提高水凝胶的溶胀性能。
的 10%、0.08%、0.12%,AA 中和度为 80%),制备 两种凝胶在充分吸水溶胀后的 SEM 图如图 6
了 P(AA-AMPS)与 P(AA-AMPS)/SA 两种水凝胶, 所示。从图 6 可看出,加入 SA 后的水凝胶网络结
考察了 SA 对水凝胶溶胀性能的影响。如图 5 所示, 构更为宽松,较大的孔道有利于水分子及重金属离
与 P(AA-AMPS)凝胶相比,相同的时间范围内, 子的渗透,能进一步提高水凝胶的溶胀性能。
P(AA-AMPS)/SA 凝胶吸水倍率较高,吸水速率前期 两种凝胶的原子力显微镜图像如图 7 所示。由
稍快,但达到饱和吸水的时间几乎相同。加入适量 图 7 可知,加入 SA 后的凝胶表面高度分布明显大
的 SA 可提高水凝胶的溶胀性能,这是因为 SA 具有 于未加 SA 的 P(AA-AMPS)凝胶,说明聚合时引入