Page 194 - 《精细化工》2021年第9期
P. 194
·1908· 精细化工 FINE CHEMICALS 第 38 卷
1/n
模型,说明 Cd(Ⅱ)在 N-MGA 上的吸附是共享电子 Freundlich 吸附等温线常数(mg/g)(L/mg) ,为与吸
对或者电子转移的化学吸附 [16] 。 附剂和重金属离子的性质、种类有关的经验常数;
1/n 用来检测吸附剂对重金属离子是否容易吸附的
表 1 N-MGA 对 Cd(Ⅱ)的吸附动力学拟合常数
Table 1 Fitting constants of adsorption kinetics for Cd(Ⅱ) 常数。
准一级动力学模型 准二级动力学模型 表 2 Langmuir 和 Freundlich 模型拟合的相关参数
k 2/〔g/(mg・ Table 2 Parameters of Langmuir and Freundlich models
–1
q e/(mg/g) R 2 k 1/min q e/(mg/g) R 2
min)〕
Langmuir 模型 Freundlich 模型
28.8 0.977 0.111 28.9 0.999 0.335 K L/
1/n
T/K Q max/(mg/g) R 2 K F/(mg/g)(L/mg) 1/n R 2
(L/mg)
2.3.2 吸附等温线模型的建立 298 539.1 0.037 0.995 52.8 0.47 0.980
分别采用 Langmuir 和 Freundlich 吸附等温线方 318 565.6 0.038 0.995 58.1 0.46 0.972
程描述 N-MGA 吸附剂对 Cd(Ⅱ)的吸附过程,吸附 338 595.4 0.041 0.995 65.7 0.45 0.981
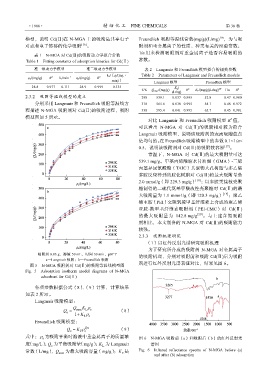
模型图如 5 所示。 2
对比 Langmuir 和 Freundlich 吸附模型 R 值,
可以看出 N-MGA 对 Cd(Ⅱ)的吸附相对较为符合
Langmuir 吸附模型,说明该吸附剂的表面吸附位点
是均匀的。在 Freundlich 吸附模型中的参数 0.1<1/n<
0.5,说明该吸附剂对 Cd(Ⅱ)的吸附较容易 [17] 。
常温下,N-MGA 对 Cd(Ⅱ)的最大吸附量可达
539.1 mg/g。甲基丙烯酸缩水甘油醚(GMA)-三烯
丙基异尿氰酸酯(TAIC)共聚物大孔树脂与多乙烯
多胺反应得到的胺化树脂对 Cd(Ⅱ)的最大吸附量是
2.0 mmol/g(即 229.3 mg/g) [18] ;以多胺类接枝壳聚
糖制得的二硫代氨基甲酸改性壳聚糖对 Cd(Ⅱ)的最
大吸附量为 1.1 mmo1/g(即 120.3 mg/g) [19] ;聚乙
烯亚胺(PEI)交联到羧甲基纤维素上合成的聚乙烯
亚胺-羧甲基纤维素吸附剂(PEI-CMC)对 Cd(Ⅱ)
的最大吸附量为 142.8 mg/g [20] 。与上述含氮吸附
剂相比,本文制备的 N-MGA 对 Cd(Ⅱ)的吸附能力
较强。
2.3.3 吸附机理研究
(1)以红外反射光谱研究吸附机理
为了研究所合成的吸附剂 N-MGA 对金属离子
吸附剂 0.03 g,溶液 50 mL,时间 30 min,pH=7 的吸附机理,分别对吸附前和吸附 Cd(Ⅱ)后为吸附
a—Langmuir 吸附;b—Freundlich 吸附
图 5 N-MGA 吸附剂对 Cd(Ⅱ)的吸附等温线模型图 剂进行红外反射光谱表征对比,结果见图 6。
Fig. 5 Adsorption isotherm model diagrams of N-MGA
adsorbent for Cd(Ⅱ)
各项参数根据公式(8)、(9)计算,计算结果
如表 2 所示。
Langmuir 吸附模型:
Q K
L e
max
Q 1 K (8)
e
Le
Freundlich 吸附模型:
Q K 1 n (9)
F e
e
式中: 为吸附平衡时溶液中重金属离子的质量浓 图 6 N-MGA 吸附前(a)和吸附后(b)的红外反射光
e
度(mg/L);Q 为平衡吸附量(mg/g);K 为 Langmuir 谱图
L
e
常数(L/mg),Q max 为最大吸附容量(mg/g);K 是 Fig. 6 Infrared reflectance spectra of N-MGA before (a)
F
and after (b) adsorption