Page 59 - 《精细化工》2022年第8期
P. 59
第 8 期 王瑞瑞: 角蛋白基药物载体材料的发展及应用探讨 ·1559·
构使角蛋白基药物载体材料能够抵御环境因素(温 的能力。目前,角蛋白基药物载体材料已作为周围
度、光、水、生物攻击等)的变化,具有其他蛋白 神经再生、伤口愈合和止血剂广泛应用于组织工程
[5]
[4]
质材料无法比拟的稳定性 。 和再生医学领域 。作为畜牧业大国之一,中国拥
有丰富的毛发资源,因此,从廉价的毛发中提取角
蛋白,开发不同形式角蛋白基药物载体材料,既能
够提高药物的活性和生物利用率,又能够增加毛发
的利用价值,还能够实现节能减排。
1 角蛋白基药物载体材料的改性方法
从毛发中提取角蛋白通常需要采用还原法、氧
化法、酶解法、离子液体法等方法破坏毛发结构中
的二硫键、氢键、范德华力等分子间相互作用力,
使角蛋白溶出。由于提取过程中角蛋白的结构在一
定程度上遭到破坏,致使其力学性能和热性能均较
差,无法与天然存在的角蛋白相媲美,极大地限制
了其作为药物载体的应用范围。因此,对角蛋白分
子结构上的活性基团进行改性处理是克服这一缺点
图 1 角蛋白的分子结构 [4] 的最有效方法。由于角蛋白分子结构中可供修饰的
[4]
Fig. 1 Molecular structure of keratin
基团有限,传统角蛋白基材料的化学改性方法通常
角蛋白分子中存在细胞粘附序列 LDV(亮氨酸- 需要使用一些具有潜在细胞毒性的化学试剂。例如:
天冬氨酸-缬氨酸)、EDS(谷氨酸-天冬氨酸-丝氨酸) 戊二醛、乙二醇缩水甘油醚等,而且改性工艺比较
和 RGD(精氨酸-甘氨酸-天冬氨酸) [6-7] ,通过细胞- 繁琐,因此,如何改进改性工艺、简化工艺流程,
配体相互作用增强了细胞和基质间的相互作用,为细 在改性过程中避免使用有毒试剂仍然是当前角蛋白
胞提供了良好的生存环境,使角蛋白基药物载体材料 基载体材料改性的研究重点。
[8]
具有优异的生物相容性 。不同于传统合成类高分子 1.1 二硫键重建
载体材料(聚苯乙烯、聚丙烯酸酯、聚乙烯醇、聚 角蛋白是含有大量半胱氨酸残基的结构蛋白,半
酸酐等),角蛋白基药物载体材料安全无害、可再生、 胱氨酸残基上的巯基可以与另一个半胱氨酸残基上
可生物降解、具有合成类材料无可比拟的可调性、 的巯基形成二硫键,二硫键的桥键作用进而使角蛋白
生物相容性和刺激响应性(温度、pH、氧化条件、 分子之间产生交联、折叠。因此,对角蛋白分子结构
特定生物分子等),是开发“智能”药物载体的理想 上的二硫键进行重建,形成分子间交联,使角蛋白具
[9]
材料 。也不同于许多传统的生物载体材料(多糖、 有高的稳定性,可赋予角蛋白基药物载体材料独特的
[2]
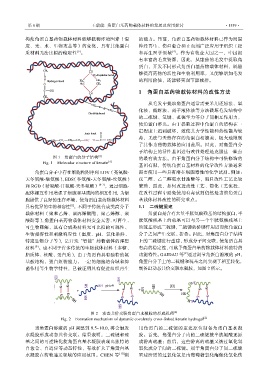
脂质体、核酸、蛋白质),由于角蛋白具有独特的氨 功能特性。GAIDAU 等 通过调节角蛋白溶液的 pH,
基酸结构,强自组装能力,一定的细胞结合域和抑 角蛋白分子上的二硫键和巯基之间实现了相互转化,
菌作用等生物学特性,已被证明具有促进组织再生 制备出动态共价交联水凝胶,如图 2 所示。
图 2 动态共价交联角蛋白水凝胶的形成机理 [2]
Fig. 2 Formation mechanism of dynamic covalently cross-linked keratin hydrogel [2]
当角蛋白溶液的 pH 调整到 9.5~10.0,将会触发 用角蛋白的二硫键的重建原位制备角蛋白基水凝
水凝胶形成动态共价交联。结果表明,二硫键和巯 胶。首先,角蛋白分子内的二硫键被半胱氨酸还原
基之间的可逆转化使角蛋白基水凝胶表现出独特的 成游离巯基;然后,这些游离的巯基又被过氧化氢
自愈合、自适应等动态特性,有效扩大了角蛋白基 氧化成分子间的二硫键。用于角蛋白分子间二硫键
水凝胶在药物递送领域的应用范围。CHEN 等 [10] 利 重建所需的过氧化氢是由葡萄糖氧化酶催化氧化伤