Page 132 - 201811
P. 132
·1918· 精细化工 FINE CHEMICALS 第 35 卷
PAA-FA 的 平均水力 学粒径为 460.8 nm ,较 化 DPBF 的 UV-Vis 谱。随着光照时间的增加,DPBF
UCNPs@TiO 2 (306.9 nm)明显增大,可能源于亲水 的吸收峰快速减弱,在最大吸收波长 414 nm 处吸收
性 PEI 和 PAA 修饰层在水中发生的溶胀。 强度的降幅分别为 76.4%和 76.7%,表明 UCNPs@TiO 2
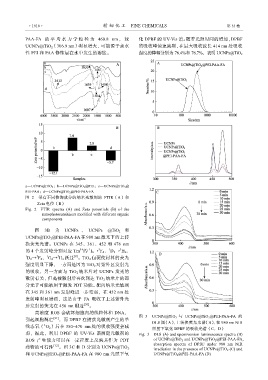
a—UCNPs@TiO 2;b—UCNPs@TiO 2@PEI;c—UCNPs@TiO 2@
PEI-PAA;d—UCNPs@TiO 2@PEI-PAA-FA
图 2 带有不同修饰成分的纳米光敏剂的 FTIR(A)和
Zeta 电位(B)
Fig. 2 FTIR spectra (A) and Zeta potentials (B) of the
nanophotosensitizers modified with different organic
components
图 3B 为 UCNPs 、 UCNPs @TiO 2 和
UCNPs@TiO 2@PEI-PAA-FA 在 980 nm激光下的上转
换荧光光谱。UCNPs 在 345、361、452 和 476 nm
1
1
3+
3
3
的 4 个发射峰分别对应 Tm 的 I 6 → F 4 、 D 2 → H 6 、
[8]
3
1
1 D 2 → F 4 、 G 4 → H 6 跃迁 。TiO 2 包覆使材料的荧光
3
强度明显下降,一方面是因为 TiO 2 对紫外区发射光
的吸收,另一方面与 TiO 2 纳米片对 UCNPs 发光的
散射有关,但是被散射后再次到达 TiO 2 纳米片的部
分光子可能被用于激发 PDT 功能。靶向纳米光敏剂
在 345 和 361 nm 发射峰进一步变弱,在 452 nm 处
发射峰明显增强,这是由于 FA 吸收了上述紫外光
后发射的荧光在 450 nm 附近 [20] 。
高浓度 ROS 会破坏细胞内的线粒体和 DNA,
引起细胞凋亡 [21] ,而 DPBF 在捕获光敏剂产生的单 图 3 UCNPs@TiO 2 与 UCNPs@TiO 2 @PEI-PAA-FA 的
DLS 图(A)、上转换荧光光谱(B)、在 980 nm NIR
1
线态氧( O 2 )后在 350~470 nm 处的吸收强度会减 照射下氧化 DPBF 的吸收光谱(C,D)
弱,据此,利用 DPBF 的 UV-Vis 谱测定光敏剂的 Fig. 3 DLS (A) and upconversion luminescence spectra (B)
ROS 产生能力可以在一定程度上反映其作为 PDT of UCNPs@TiO 2 and UCNPs@TiO 2 @PEI-PAA-FA,
药物的可行性 [12] 。图 3C 和 D 分别为 UCNPs@TiO 2 absorption spectra of DPBF under 980 nm NIR
irradiation in the presence of UCNPs@TiO 2 (C) and
和 UCNPs@TiO 2 @PEI-PAA-FA 在 980 nm 光照下氧 UCNPs@TiO 2 @PEI-PAA-FA (D)