Page 60 - 201812
P. 60
·2028· 精细化工 FINE CHEMICALS 第 35 卷
分解的 γ-Al 2 O 3 改性工业活性 ZnO 和碱式碳酸锌分
解活性 ZnO 制备的氧化锌基脱硫剂(Z3 和 Z7)脱
除 H 2 S 的穿透曲线如图 6 所示。
图 5 Z2 和 Z6 的 H 2 S 穿透曲线
Fig. 5 Breakthrough curves of H 2 S for Z2 and Z6
对比图 5 与图 2 可以看出,添加碱性助剂 K 2 CO 3
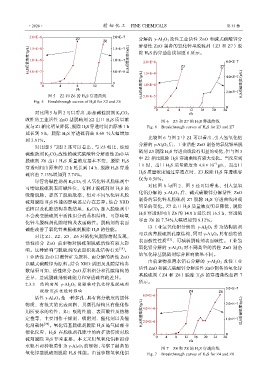
改性的工业活性 ZnO 基脱硫剂 Z2 出口 H 2 S 质量浓 图 6 Z3 和 Z7 的 H 2 S 穿透曲线
度与 Z1 相比明显降低,脱除 H 2 S 穿透时间由原来 1 h Fig. 6 Breakthrough curves of H 2 S for Z3 and Z7
延长到 5 h,脱除 H 2 S 穿透硫容由 0.60 %大幅增加
比较图 6 与图 2 中 Z1 可以看出,引入氢氧化铝
到 2.91%。
分解的 γ-Al 2O 3 后,工业活性 ZnO 制备的氧化锌基脱
对比图 5 与图 2 还可以看出,与 Z5 相比,添加
硫剂 Z3 脱除 H 2S 穿透曲线没有明显的变化,但与图 5
碱性助剂 K 2 CO 3 改性的碱式碳酸锌分解活性 ZnO 基
中 Z2 相比脱除 H 2S 穿透曲线有较大变化。当反应到
脱硫剂 Z6 出口 H 2 S 质量浓度基本不变,脱除 H 2 S
–7
1 h 时,出口 H 2S 质量浓度为 4.8×10 g/L,当出口
穿透时间由原来的 12 h 延长到 14 h,脱除 H 2 S 穿透
H 2 S 质量浓度超过穿透点时,Z3 脱除 H 2 S 穿透硫容
硫容由 7.13%增加到 7.74%。
仅为 0.56%。
尽管将碱性助剂 K 2 CO 3 引入氧化锌基脱硫剂中
对比图 6 与图 2、图 5 还可以看出,引入氢氧
可增加脱硫剂表面碱性位,有利于脱硫剂对 H 2 S 的
化铝分解的 γ-Al 2 O 3 后,碱式碳酸锌分解活性 ZnO
吸附脱除,提高了脱硫效率,但对不同氧化锌基脱
制备的氧化锌基脱硫剂 Z7 脱除 H 2 S 穿透曲线出现
硫剂脱除 H 2 S 性能的影响还是存在差异。结合 XRD
明显的变化。Z7 出口 H 2 S 质量浓度明显降低,脱除
谱图以及孔隙结构参数结果,K 2 CO 3 加入脱硫剂中
H 2 S 穿透时间由 Z6 的 14.0 h 延长到 16.5 h,穿透硫
不会改变脱硫剂中活性组分的晶相结构,可影响氧
容由 Z6 的 7.74%大幅增加到 9.12%。
化锌基脱硫剂孔隙结构及表面碱性。脱硫剂的表面
以工业氢氧化铝分解的 γ-Al 2 O 3 作为结构助剂
碱性改善了氧化锌基脱硫剂脱除 H 2 S 的性能。
可以改善脱硫剂孔隙结构,同时 γ-Al 2 O 3 具有独特的
对比 Z1、Z2、Z5、Z6 对硫化氢脱除情况发现,
表面酸性性质 [21] ,可减弱脱硫剂表面碱性。工业氢
活性组分 ZnO 前驱物对脱硫剂脱硫活性有较大影
响。这种影响与脱硫剂的表面积和孔结构有关 [19] 。 氧化铝分解的 γ-Al 2 O 3 对不同类型的活性 ZnO 制备
的氧化锌基脱硫剂综合影响效果不同。
工业活性 ZnO 以菱锌矿为原料,而分解的活性 ZnO
由前驱物拟薄水铝石分解的 γ-Al 2 O 3 改性工业
以碱式碳酸锌为原料。结合 XRD 谱图及孔隙结构参
活性 ZnO 和碱式碳酸锌分解活性 ZnO 制备的氧化锌
数结果可知,活性组分 ZnO 原料组分和孔隙结构的
基脱硫剂(Z4 和 Z8)脱除 H 2 S 的穿透曲线如图 7
差异,造成脱硫剂吸硫能力和穿透硫容的差异。
所示。
2.3.3 结构助剂 γ-Al 2 O 3 前驱物对氧化锌基脱硫剂
脱除 H 2 S 性能的影响
活性 γ-Al 2 O 3 是一种多孔、具有高分散度的固体
物质,有很大的比表面积,其微孔结构具有催化作
用所要求的特性,如:吸附性能、表面酸性及热稳
定性等,主要用作干燥剂、吸附剂、催化剂以及催
化剂载体 [20] 。氧化锌基脱硫剂脱除 H 2 S 是气固相非
催化反应,H 2 S 在脱硫剂孔隙中的内扩散传质对脱
硫剂脱除 H 2 S 非常重要。本文采用氢氧化铝和拟薄
水铝石两种物质作为 γ-Al 2 O 3 前驱物,考察了制备的
图 7 Z4 和 Z8 的 H 2 S 穿透曲线
氧化锌基脱硫剂脱除 H 2 S 性能。由前驱物氢氧化铝 Fig. 7 Breakthrough curves of H 2 S for Z4 and Z8