Page 145 - 201902
P. 145
第 2 期 尚宏周,等: 温敏型表面离子印迹聚合物的制备及性能 ·311·
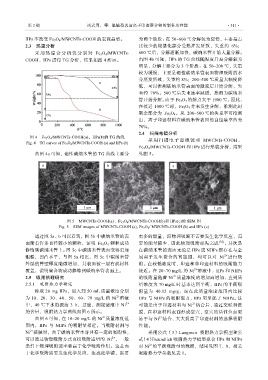
IIPs 不改变 Fe 3 O 4 /MWCNTs-COOH 的表面晶型。 为两个阶段:在 50~600 ℃分解较为缓慢,主要是占
2.3 热重分析 比较少的羧基化部分受热挥发所致,失重约 6%;
采用热综合 分析仪分别 对 Fe 3 O 4 /MWCNTs- 600 ℃后,分解逐渐加快,碳纳米管开始大量分解。
COOH、IIPs 进行 TG 分析,结果如图 4 所示。 由图 4b 可知,IIPs 的 TG 曲线随温度升高分解较为
明显,分解主要分为 3 个阶段:在 50~200 ℃,失重
较为缓慢,主要是磁性碳纳米管表面物理吸附的水
分蒸发所致,失重约 8%;200~500 ℃质量大幅度降
低,可以推测碳纳米管表面的凝胶层开始分解,失
重约 70%;500 ℃后失重速率减缓,推测为碳纳米
管开始分解。由于 Fe 3 O 4 的熔点大于 1000 ℃,因此,
在接近 1000 ℃时,Fe 3 O 4 并未发生分解,推测此时
剩余部分为 Fe 3 O 4 。从 200~500 ℃的失重率可推测
出,离子印迹材料在碳纳米管表面的自组装率约为
70%。
2.4 扫描电镜分析
图 4 Fe 3 O 4 /MWCNTs-COOH(a)、IIPs(b)的 TG 曲线
Fig. 4 TG curves of Fe 3 O 4 /MWCNTs-COOH (a) and IIPs (b) 采用扫描电子显微镜对 MWCNTs-COOH 、
Fe 3 O 4 /MWCNTs-COOH 和 IIPs 进行形貌分析,结果
由图 4a 可知,磁性碳纳米管的 TG 曲线主要分 见图 5。
图 5 MWCNTs-COOH(a)、Fe 3 O 4 /MWCNTs-COOH(b)和 IIPs(c)的 SEM 图
Fig. 5 SEM images of MWCNTs-COOH (a), Fe 3 O 4 / MWCNTs-COOH (b) and IIPs (c)
通过图 5a、b 可以看到,图 5b 中碳纳米管的表 更多的能量,而物理吸附不需要发生化学反应,需
面附着许多直径较小的颗粒,证明 Fe 3 O 4 颗粒成功 要的能量较少,因此物理吸附率先完成 [32] ;其次是
修饰到碳纳米管上。图 5c 中碳纳米管表面变得更加 在碳纳米管的表面无论是 IIPs 或 NIIPs 都存在与金
2+
粗糙,凹凸不平,与图 5a 相比,图 5c 中碳纳米管 属离子发生鳌合的官能团,均可以对 Ni 进行吸
外层的管壁厚度略微增加,其表面被一层有机材料 附。在较低浓度时,印迹和非印迹材料的吸附能力
2+
覆盖,说明聚合物成功修饰到碳纳米管表面上。 接近。在 20~70 mg/L 的 Ni 溶液中,IIPs 和 NIIPs
2+
2.5 吸附机理研究 的吸附量随着 Ni 质量浓度的增加而增加,直到质
2.5.1 吸附热力学研究 量浓度为 70 mg/L 时基本达到平衡,IIPs 的平衡吸
称取 20 mg IIPs,加入到 50 mL 质量浓度分别 附量为 40.12 mg/g,而在此质量浓度范围内比较
2+
为 10、20、30、40、50、60、70 mg/L 的 Ni 溶液 IIPs 与 NIIPs 的吸附能力,IIPs 明显优于 NIIPs。这
2+
中,40 ℃下水浴振荡 3 h,过滤,测定滤液中 Ni 2+ 可能是由于印迹材料与 Ni 结合后,通过交联和洗
的含量,吸附热力学曲线如图 6 所示。 脱,在印迹材料表面形成空穴,空穴的活性位点更
2+
2+
由图 6 可知,在 10~20 mg/L 的 Ni 质量浓度范 易于与 Ni 结合,大大提高了印迹材料的选择吸附
围内,IIPs 与 NIIPs 的吸附量相近。当吸附材料与 性能。
2+
Ni 接触时,由于碳纳米管本身具有一定的吸附性, 采用公式(3)Langmuir 吸附热力学模型和公
2+
可以通过物理吸附方式直接吸附适量的 Ni ,一般 式(4)Freundlich 吸附热力学模型拟合 IIPs 和 NIIPs
2+
条件下物理吸附速率要高于化学吸附作用。这是由 对 Ni 的平衡吸附量的数据,结果见图 7、8,相关
于化学吸附需要发生化学反应,生成化学键,需要 吸附热力学参数见表 1。