Page 108 - 《精细化工》2020年第9期
P. 108
·1822· 精细化工 FINE CHEMICALS 第 37 卷
2.2 Au-Cur NPs 的吸附率和载药率 姜黄素水溶液的 Zeta 电位为(–31.80 ± 6.22) mV,
金纳米颗粒与姜黄素疏水结合后通过离心纯 金纳米颗粒分散液为(–4.03 ± 0.61) mV,而 Au-Cur
化,相应的上清液中姜黄素的含量可根据姜黄素的 NPs 为(–10.82 ± 4.58)mV,介于姜黄素水溶液与
2
标准曲线(R =0.9997)计算。根据所得上清液中姜 金纳米颗粒分散液之间。该结果进一步证实了 Au-Cur
黄素的含量,分析得到 Au-Cur NPs 中姜黄素的吸附 NPs 中姜黄素在金纳米颗粒表面的负载。
率为(86.85%±3.54%),载药率为(20.25%±0.88%)。 2.3 Au-Cur@RBC 的形貌与表征
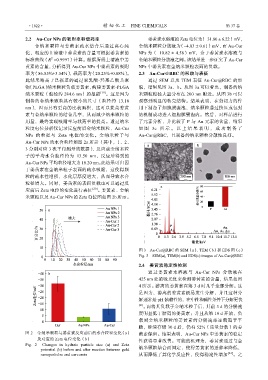
此结果略高于已报道的通过聚乳酸-羟基乙酸共聚 通过 SEM 以及 TEM 表征 Au-Cur@RBC 的形
物(PLGA)纳米颗粒负载姜黄素,构建姜黄素-PLGA 貌,结果见图 3a、b。从图 3a 可以看出,制备的纳
纳米颗粒(粒径约 284.6 nm)的报道 [19] 。这是因为 米颗粒粒径大量分布在 200 nm 附近。从图 3b 可以
制备的金纳米颗粒具有较小的尺寸(粒径约 13.18 观察到明显的核壳结构。结果表明,在剪切力的作
nm),因而具有更高的比表面积,这可以提高姜黄 用下制备了细胞膜囊泡,纳米颗粒通过挤压或包封
素与金纳米颗粒的结合几率,从而减少纳米颗粒的 的机制成功进入细胞膜囊泡内。然后,对样品进行
用量,最终实现吸附率与载药率的提高。通过纳米 了元素分析,并比较了 P 与 Au 元素的含量,结果
粒度电位分析仪记录反应前后金纳米颗粒、Au-Cur 如图 3c 所 示。以上结果表明,成功制备了
NPs 的粒径与 Zeta 电位的变化。金纳米粒子与 Au-Cur@RBC,且制备的纳米颗粒分散性良好。
Au-Cur NPs 的水合粒径如图 2a 所示(其中,1、2、
3 分别对应 3 次平行测量的数据),反应前金纳米粒
子的平均水合粒径约为 13.50 nm,反应后得到的
Au-Cur NPs 平均粒径增大为 18.20 nm。此结果可归因
于姜黄素在金纳米粒子表面的疏水吸附,这使得颗
粒的疏水性增强,水化层厚度增大,从而导致水合
粒径增大。同时,姜黄素的表面负载也可以通过反
应前后 Zeta 电位的变化进行表征 [20] 。姜黄素、金纳
米颗粒以及 Au-Cur NPs 的 Zeta 电位图如图 2b 所示。
图 3 Au-Cur@RBC 的 SEM(a)、TEM(b)和 EDS 图(c)
Fig. 3 SEM(a), TEM(b) and EDS(c) images of Au-Cur@RBC
2.4 姜黄素稳定性检测
通过姜黄素水溶液与 Au-Cur NPs 分散液在
425 nm 处的吸光度来检测姜黄素的含量,结果如图
4 所示。游离的姜黄素在第 3 d 时几乎全部分解。这
是因为,游离的姜黄素极易发生分解,并且这种分
解通常是 pH 依赖性的,在中性和碱性条件下分解更快
[21] 。而将其负载于金纳米粒子后,其前 3 d 的分解速
度明显低于游离的姜黄素;并且从第 10 d 开始,负
载到金纳米颗粒的姜黄素的分解速率逐渐趋于平
稳,继续存储 30 d 后,仍有 52%(质量分数)的姜
图 2 金纳米颗粒与姜黄素反应前后的水合粒径变化(a) 黄素保留。结果表明,Au-Cur NPs 中姜黄素的稳定
及对应的 Zeta 电位变化(b) 性获得显著改善。可能的机理为,姜黄素通过与金
Fig. 2 Changes in hydrate particle size (a) and Zeta
potential (b) before and after reaction between gold 纳米颗粒结合而固定,使得姜黄素的迁移率降低,
nanoparticles and curcumin 从而降低了其化学反应性,使得稳定性增加 [22] 。之