Page 58 - 《精细化工》2020年第9期
P. 58
·1772· 精细化工 FINE CHEMICALS 第 37 卷
2.4 选择性和竞争实验
决定荧光探针性能的一个重要因素是其选择
2+
性。在多种干扰离子存在下检测 P1 对 Cu 的专一
选择性,结果如图 3 所示。这些干扰离子对 P1 几乎
2+
不响应,然后加入 Cu ,荧光强度没有发生变化。
2+
结果表明,P1 对 Cu 具有高选择性。
+
2+
–
+
2+
1—空白; 2—Ca ; 3—K ; 4—Na ; 5—Mg ; 6—H 2S; 7—HSO 3;
–
2–
–
+
–
2–
2+
8—SO 3 ; 9—SO 4 ; 10—Fe ; 11—NH 4; 12—F ; 13—Cl ; 14—Br ;
–
15—I ; 16—H 2O 2; 17—半胱氨酸; 18—高半胱氨酸; 19—乙二胺;
20—氨水; 21—苯胺; 22—L-苯丙氨酸; 23—脯氨酸; 24—L-赖氨
酸; 25—L-丝氨酸
图 3 不同干扰离子对 P1 的影响
Fig. 3 Effect of different interfering ions on P1
2.5 机理研究
2+
P1 对 Cu 的识别机理是 2-吡啶甲酸酯与 Cu 2+
络合、水解,生成化合物Ⅴ和化合物Ⅵ,机理示意
图见图 4。采用液相色谱-质谱联用仪对 P1 与 Cu 2+
的 PBS 缓冲溶液进行检测,结果如图 5 所示。m/Z =
–
327.26 为化合物Ⅴ的分子离子峰[M–H] ,m/Z =
2+
186.17 为化合物Ⅵ的分子离子峰。P1 对 Cu 的响应
机理是基于 2-吡啶甲酸基团的水解。
2+
图 4 P1 与 Cu 的响应机理示意图
2+
Fig. 4 Sensing mechanism for reaction of P1 with Cu
2+
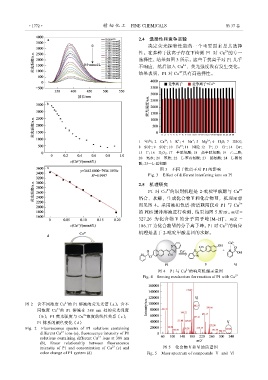
图 2 含不同浓度 Cu 的 P1 溶液的荧光光谱(a);含不
2+
同浓度 Cu 的 P1 溶液在 388 nm 处的荧光强度
2+
(b);P1 荧光强度与 Cu 浓度的线性关系(c);
P1 体系的颜色变化(d)
Fig. 2 Fluorescence spectra of P1 solutions containing
2+
different Cu ions (a), fluorescence intensity of P1
2+
solutions containing different Cu ions at 388 nm
(b), linear relationship between fluorescence
intensity of P1 and concentration of Cu 2+ (c) and 图 5 化合物Ⅴ和Ⅵ的质谱图
color change of P1 system (d) Fig. 5 Mass spectrum of compounds Ⅴ and Ⅵ