Page 167 - 《精细化工》2021年第3期
P. 167
第 3 期 陈秀琼,等: 基于 UGI 反应制备海藻酸衍生物及其载药微胶囊的释药性 ·587·
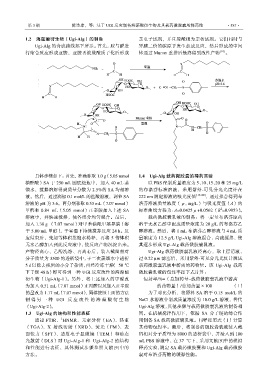
1.2 海藻酸衍生物(Ugi-Alg)的制备 亲电子试剂,并且羧酸根为亲核试剂。它们同时与
Ugi-Alg 的合成路线如下所示。首先,胺与醛进 异腈二价的碳原子发生加成反应,然后形成的中间
行缩合反应形成亚胺,亚胺再被羧酸质子化后形成 体通过 Mumm 重排后最终得到改性产物 [10] 。
具体步骤如下:首先,准确称取 1.0 g(5.05 mmol 1.4 Ugi-Alg 载药微胶囊的释药实验
糖醛酸)SA 于 250 mL 圆底烧瓶中,加入 40 mL 蒸 以 PBS 配制质量浓度为 5、10、15、20 和 25 mg/L
馏水,搅拌溶解得到质量分数为 2.5%的 SA 均相溶 的布洛芬标准溶液,采用紫外-可见分光光度计在
液。然后,通过滴加 0.1 mol/L 的盐酸溶液,调节 SA 222 nm 测定溶液的吸光度值 [19-20] ,通过拟合得到布
溶液的 pH 为 3.6。再分别移取 0.53 mL(7.07 mmol) 洛芬溶液质量浓度(ρ, mg/L)与吸光度值(A)的
2
甲醛和 0.84 mL(5.05 mmol)正辛胺加入上述 SA 标准曲线方程为:A=0.0425ρ+0.0562 (R =0.9953)。
溶液中,并快速搅拌,使各组分均匀混合。最后, 载药微胶囊乳液的制备:将一定量布洛芬原药
加入 1.38 g (7.07 mmol)对甲苯磺酰甲基异腈(溶 溶于无水乙醇中配成质量浓度为 20 g/L 的布洛芬乙
于 5.00 mL 甲醇),于室温下持续搅拌反应 24 h。反 醇溶液。然后,将 1 mL 布洛芬乙醇溶液与 4 mL 质
应结束后,先加等体积蒸馏水稀释,再将 5 倍体积 量浓度为 12.5 g/L Ugi-Alg 溶液混合,高速搅拌,使
无水乙醇加入到此反应液中,使反应产物沉淀出来。 其逐步形成 Ugi-Alg 载药微胶囊乳液。
产物经离心、乙醇洗涤、再离心后,装入截留相对 Ugi-Alg 载药微胶囊乳液经离心,取上层清液,
分子质量为 3500 的透析袋中,于二次蒸馏水中透析 过 0.22 µm 滤塞后,采用紫外-可见分光光度计测试
5 d 以除去残留的小分子杂质,再经冷冻干燥(–50 ℃ 载药微胶囊乳液中游离的药物量。该 Ugi-Alg 载药
下干燥 48 h)即可得到一种 UGI 反应改性的海藻酸 微胶囊乳液的包封率按下式计算:
衍生物(Ugi-Alg-1)。另外,将上述加入的甲醛改 包封率/%=(总加药量–载药微胶囊乳液中游离
为加入 0.51 mL(7.07 mmol)正丙醛以及加入正辛胺 的药物量)/总加药量×100 (1)
的量改为 1.17 mL(7.07 mmol),同样按照上面的方法 为了对比分析,将原料 SA 溶于 0.15 mol/L 的
制得另一种 UGI 反 应改性的海藻酸衍生物 NaCl 水溶液中制成质量浓度为 10.0 g/L 溶液,替代
(Ugi-Alg-2)。 Ugi-Alg 溶液,其他步骤与载药微胶囊乳液的制备相
1.3 Ugi-Alg 的结构和性能表征 同。在机械搅拌作用下,依据 SA 分子链的缔合作
1
通过 FTIR、 HNMR、元素分析(EA)、热重 用制备 SA 载药微胶囊乳液。同样按照式(1)计算
(TGA)、X 射线衍射(XRD)、荧光(FM)、表 其药物包封率。最后,将制备的微胶囊乳液装入截
面张力(SFT)、透射电子显微镜(TEM)和动态 留相对分子质量为 8000 的透析袋中,并浸入到 100
光散射(DLS)对 Ugi-Alg-1 和 Ugi-Alg-2 的结构 mL PBS 溶液中,在 37 ℃下,采用文献[9]中的模拟
和性能进行表征,具体测试步骤参照文献[9]中的 释药实验,测定 SA 载药微胶囊和 Ugi-Alg 载药微胶
方法。 囊对布洛芬药物的缓释性能。