Page 96 - 《精细化工》2022年第7期
P. 96
·1382· 精细化工 FINE CHEMICALS 第 39 卷
等温常数,L/mg;K F 为 Freundlich 等温常数,(mg/g)
由表 1 可知,拟一级动力学模型计算出的 q e, cal
1/n
比拟二级动力学模型更接近 q e, exp。而拟二级动力学 (L/mg) 。
2
模型的相关系数(R )高于拟一级动力学模型,说明拟
–
表 2 BT-g-CMC1.0 水凝胶在不同温度下对 H 2 PO 4 吸附等
二级动力学模型可以更好地描述 BT-g-CMC 水凝胶
温系数
–
对 H 2 PO 4 的吸附过程。 Table 2 Isotherm parameters for H 2 PO 4 adsorption on BT-
–
–
2.4 不同温度下 H 2PO 4 在 BT-g-CMC1.0 上的等温 g-CMC1.0 hydrogels at various temperatures
吸附 Langmuir 模型 Freundlich 模型
– K F/[(mg
按照 1.4.2 节实验条件,测定了不同温度下 H 2PO 4 T/K 2 2
q max/(mg/g) K L/(L/mg) R n /g)(L/m R
在 BT-g-CMC1.0 上的吸附等温线,结果见图 7。 g) ]
1/n
298 123.5 0.0205 0.9605 1.4678 4.2892 0.9654
308 125.0 0.0166 0.9457 1.4209 3.5733 0.9666
318 112.4 0.0143 0.9298 1.4440 3.0334 0.9761
由表 2 可知,Freundlich 等温线模型更适合描述
–
H 2 PO 4 的吸附过程,表明化学吸附在吸附过程中起
主导作用,同时也说明 BT-g-CMC1.0 在吸附过程中
–
提供了异质吸附面,从而在随后的 H 2 PO 4 吸附过程
中导致多重吸附平衡。
2.5 吸附机理
为了进一步阐明 BT-g-CMC1.0 的吸附机理,进
–
行了吸附 H 2PO 4 前后的 BT-g-CMC1.0 水凝胶 XPS 分
–
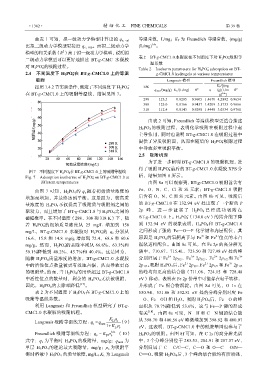
图 7 不同温度下 H 2 PO 4 在 BT-g-CMC1.0 上的吸附等温线
–
Fig. 7 Adsorption isotherms of H 2 PO 4 on BT-g-CMC1.0 at 析,结果如图 8 所示。
different temperatures 由图 8a 可以观察到,BT-g-CMC1.0 吸附前含有
–
由图 7 可知,H 2PO 4 的 q e 随着初始质量浓度的 Fe、O、N、C、Cl 和 Si 元素;BT-g-CMC1.0 吸附
增加而增加,并最终达到平衡。这是因为,较高质 后含有 O、N、C 和 Si 元素。由图 8b 可见,吸附后
–
量浓度的 H 2 PO 4 不仅提高了吸附质与吸附剂之间的 的 BT-g-CMC1.0 在 132.94 eV 处出现了一个新的 P
–
–
驱动力,而且增加了 BT-g-CMC1.0 与 H 2 PO 4 之间的 2p 峰 , 进 一 步证实了 H 2 PO 4 已经 成功吸 附在
–
碰撞概率。在不同温度(298、308 和 318 K)下,随 BT-g-CMC1.0 上。H 2PO 4(134.0 eV)的结合能下降
–
–
着 H 2PO 4 的初始质量浓度从 25 mg/L 增加到 150 到 132.94 eV 的现象表明,H 2PO 4 和 BT-g-CMC1.0
–
mg/L,BT-g-CMC1.0 水凝胶对 H 2PO 4 的 q e 分别从 之间形成了强的 Fe—O—P 化学键和内层配位,其
–
2+
3+
16.6、15.8 和 14.8 mg/g 增加到 72.4、68.6 和 60.6 原因是 H 2 PO 4 的氧阴离子与 Fe 和 Fe 位点的未占
–
mg/g。然而,H 2PO 4 的去除率则从 66.6%、63.3%和 据轨道相配位。由图 8c 可见,在 Fe 2p 的高分辨光
59.1%降低到 48.2%、45.7%和 40.4%。这是因为, 谱中,710.67、715.41、723.50 和 727.98 eV 处的峰
2+
2+
3+
–
随着 H 2 PO 4 质量浓度的增加,BT-g-CMC1.0 水凝胶 分别归属于 Fe 2p 3/2 、Fe 2p 3/2 、Fe 2p 1/2 和 Fe 3+
2+
–
3+
2+
中的活性位点数量被更有效地占据,从而导致更高 2p 1/2 。吸附 H 2 PO 4 后,Fe 2p 3/2 、Fe 2p 1/2 和 Fe 2p 1/2
–
的吸附量。然而,当 H 2PO 4 的用量超过 BT-g-CMC1.0 的峰均向更高的结合能(711.08、724.15 和 728.48
–
中活性位点的数量时,剩余的 H 2 PO 4 无法被吸附, eV)移动,表明在 Fe 2p 价带中可能存在电子转移,
–
因此,H 2PO 4 的去除率降低 [17] 。 并形成了 Fe 配合物沉淀。由图 8d 可见,O 1s 在
–
表 2 为不同温度下 H 2PO 4 在 BT-g-CMC1.0 上的 530.94、531.86 和 532.81 eV 处的分峰分别对应 Fe
–
吸附等温线参数。 —O、Fe—OH 和 H 2 O。吸附 H 2 PO 4 后,Fe—O 的峰
利用 Langmuir 和 Freundlich 模型研究了 BT-g- 面积从 70.7%降低到 53.6%,这与 Fe—P 键的形成
CMC1.0 水凝胶的吸附机理。 有关 [18] 。由图 8e 可见,N—H 和 C—N 键的结合能
K 从 398.70 和 400.56 eV 略微增加到 398.92 和 400.97
Langmuir 吸附等温线方程: q q max Le (9)
e
1 K eV,这表明,BT-g-CMC1.0 中的酰胺基团也参与了
Le
–
Freundlich 吸附等温线方程:q K 1/n (10) H 2 PO 4 的吸附。由图 8f 可知,在 C 1s 的高分辨光谱
F e
e
–
式中:q e 为平衡时 H 2 PO 4 的吸附量,mg/g;q max 为 中,3 个分峰分别位于 283.53、284.91 和 287.57 eV,
–
单层 H 2 PO 4 的理论最大吸附量,mg/g;ρ e 为吸附平 分别归属于 C=C/C—C,C—O 和 O—C=O/N—
–
–
衡时溶液中 H 2PO 4 的质量浓度,mg/L;K L 为 Langmuir C=O。吸附 H 2 PO 4 后,3 个峰的结合能均有所增强,