Page 228 - 《精细化工》2023年第11期
P. 228
·2540· 精细化工 FINE CHEMICALS 第 40 卷
由图 6a 可以看出,PEI-SBC/Mt 和 SBC/Mt 的 吸附时间为 5~25 min 时,平衡吸附量增长放缓。
N 2 吸附曲线符合Ⅳ型等温线,是典型的介孔类吸附 这是因为,吸附剂表面活性位点基本被占据。所以
材料。根据Ⅳ型等温线特征分析,在临界温度时, 100 min 后吸附基本达到平衡。因此,平衡吸附时
N 2 在吸附剂表面发生单层吸附,当单层吸附达到饱 间为 100 min。
和时,开始在多层吸附。如图 6b 所示,PEI-SBC/Mt
和 SBC/Mt 的孔径主要分布在 2~20 nm 之间。根据
介孔材料的定义,两种材料孔径均分布在 2~50 nm
之间,属于介孔材料 [21] 。而且 PEI-SBC/Mt 比 SBC/Mt
的孔径和孔体积都有所减小。
2.2 PEI-SBC/Mt 对 Cd(Ⅱ)吸附分析
2.2.1 溶液初始 pH 的影响
溶液的初始 pH 影响金属离子在溶液中的存在
形式和吸附剂的表面电荷分布,对吸附过程有重要
[22]
的影响 。在 25 ℃、Cd(Ⅱ)初始质量浓度为 150 mg/L、
吸附时间 120 min 的条件下,使用 0.1 g PEI-SBC/Mt
置于含 100 mL Cd(Ⅱ)溶液锥形瓶中,于恒温水浴振
荡器中振荡,考察溶液初始 pH 对 Cd(Ⅱ)平衡吸附
量的影响,结果如图 7a 所示。由图 7a 可知,在较
低 pH 下,PEI-SBC/Mt 吸附剂对 Cd(Ⅱ)的吸附能力
+
较低,这是因为,低 pH 下 H 浓度较高,而此时镉
2+
主要以 Cd 的形式存在,两者之间存在竞争吸附;
+
同时吸附剂上的—NH 3 也容易质子化为 NH 4 ,产生
静电斥力,从而影响吸附效果。随着 pH 的增加,
PEI-SBC/Mt 表面正电荷减少,吸附量进一步增加,
pH=6 时吸附达到最大平衡吸附量,为 125 mg/g,pH
继续增加平衡吸附量反而下降,主要是因为生成了
Cd(OH) 2 影响了 PEI-SBC/Mt 对 Cd(Ⅱ)的吸附。因此,
Cd(Ⅱ)溶液的最佳初始 pH 为 6。
2.2.2 Cd(Ⅱ)初始质量浓度的影响
在 25 ℃、pH=6、吸附时间 120 min 条件下,
将 0.1 g PEI-SBC/Mt 浸入 Cd(Ⅱ)溶液(100 mL),
于恒温水浴振荡器中振荡,考察 Cd(Ⅱ)初始质量浓
度(50~1000 mg/L)下 PEI-SBC/Mt 的吸附效果,结
果如图 7b 所示。由图 7b 可知,平衡吸附量随 Cd(Ⅱ)
初始质量浓度的增加而增大。当 Cd(Ⅱ)初始质量浓度
达到 450 mg/L 时,平衡吸附量趋于稳定,这可能是球
形吸附剂所能达到的最大平衡吸附量,为 235 mg/g。
2.2.3 吸附时间的影响
在 25 ℃、pH=6 条件下,将 0.1 g PEI-SBC/Mt
放入 100 mL 含 Cd(Ⅱ)溶液的锥形瓶中,于恒温水
浴振荡器中振荡,考察 PEI-SBC/Mt 在不同 Cd(Ⅱ)
初始质量浓度(150、300、450 mg/L)下平衡吸附
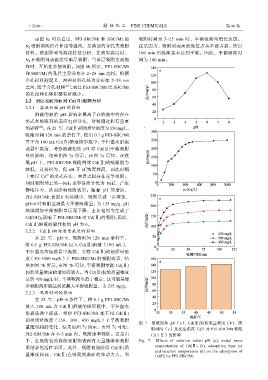
图 7 溶液初始 pH(a)、Cd(Ⅱ)初始质量浓度(b)、吸
量随时间的变化,结果如图 7c 所示。由图 7c 可知, 附时间(c)及反应温度(d)对 PEI-SBC/Mt 吸附
PEI-SBC/Mt 在 0~5 min 内,吸附速率较快。这是由 Cd(Ⅱ)的影响
于,在吸附初始阶段吸附剂表面有大量能够和吸附 Fig. 7 Effects of solution initial pH (a), initial mass
质结合的活性基团。此外,吸附初始阶段 Cd(Ⅱ)质 concentration of Cd(Ⅱ) (b), adsorption time (c)
and reaction temperature (d) on the adsorption of
量浓度较高,Cd(Ⅱ)在吸附剂表面的驱动力大。当 Cd(II) by PEI-SBC/Mt