Page 230 - 《精细化工》2023年第11期
P. 230
·2542· 精细化工 FINE CHEMICALS 第 40 卷
2.6 吸附机理分析
基于上述的表征与分析结果,本文提出可能的
吸附机理。重金属在吸附剂表面的吸附取决于表面
积、孔隙率、静电相互作用等因素。Cd(Ⅱ)在 PEI-
SBC/Mt 上的吸附符合准二级动力学模型,吸附剂表
面基团与带正电荷的 Cd(Ⅱ)通过共价电子方式形成
配体而发生螯合,表面的吸附位点数量是影响吸附
的重要因素。CaCO 3 作为致孔剂增加了 PEI-SBC/Mt
的吸附位点和比表面积,SMt 和 PEI 的加入为 PEI-
SBC/Mt 引入了羧基和氨基,进一步增加了活性位
图 9 Langmuir 等温吸附曲线(a)及 Freundlich 等温吸 点。在较低 pH 下,PEI-SBC/Mt 表面氨基质子化产
附曲线(b) 生正电荷与 Cd(Ⅱ)发生静电排斥导致吸附量较低,
Fig. 9 Langmuir isothermal adsorption curves (a) and +
Freundlich isothermal adsorption curves (b) 在较高 pH 下,镉元素以 Cd(OH) 2 、Cd(OH) 和
–
Cd(OH) 3 的形式存在,因此,PEI-SBC/Mt 在 pH=6
表 3 PEI-SBC/Mt 在不同温度下吸附 Cd(Ⅱ)的吸附等温模 左右时的吸附效果最佳。
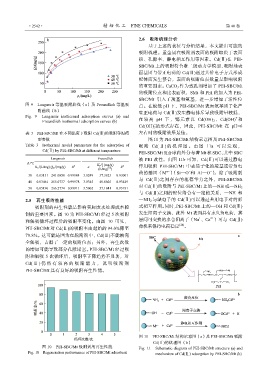
型参数 图 11 为 PEI-SBC/Mt 结构示意图及 PEI-SBC/Mt
Table 3 Isothermal model parameters for the adsorption of 吸附 Cd( Ⅱ ) 的机理 图。由 图 11a 可以发现,
Cd(Ⅱ) by PEI-SBC/Mt at different temperature
PEI-SBC/Mt 复合球内外分布着 Mt 和 SBC,其中 SBC
Langmuir Freundlich 被 PEI 改性。由图 11b 可知,Cd(Ⅱ)可以通过静电
θ/℃ K F/[ (mg/g)
2
K L/(L/mg) Q m/(mg/g) R n 1/n R 2 作用吸附 PEI-SBC/Mt 中去质子化的羧基或带负电
(L/mg) ]
n–
–
–
荷的基团(M )(Si—O 和 Al—O )。除了吸附剂
30 0.03131 241.0850 0.99984 3.0249 37.3623 0.93001
与 Cd(Ⅱ)之间存在的范德华力之外,PEI-SBC/Mt
40 0.03461 255.0737 0.99978 3.0345 40.8605 0.93429
50 0.05196 266.2774 0.99911 3.5062 57.1841 0.93181 对 Cd(Ⅱ)的吸附与 PEI-SBC/Mt 上的—NH 或—NH 2
与 Cd(Ⅱ)之间的配位络合有一定的关系,—NH 和
2.5 再生吸附性能 —NH 2 与缺电子的 Cd(Ⅱ)可以通过共用电子对的形
吸附剂的再生性能是影响实际废水处理成本控 式相互作用。同时,PEI-SBC/Mt 上的—OH 和 Cd(Ⅱ)
制的重要因素。图 10 为 PEI-SBC/Mt 经过 5 次吸附 发生阳离子交换,此外 Mt 表面具有永久负电荷,其
+
2+
和解吸循环过程后的吸附率变化。由图 10 可见, 层间可交换的水合阳离子(Na 、Ca )可与 Cd(Ⅱ)
PEI-SBC/Mt 对 Cd(Ⅱ)的吸附率由起始的 94.0%降至 替换来保持电荷稳定 [24] 。
79.8%。这可能是因为在脱附剂中,Cd(Ⅱ)不能被完
全解吸,占据了一定的吸附位点;另外,再生次数
的增加可能导致部分孔隙堵塞。PEI-SBC/Mt 经过吸
附和解吸 5 次循环后,吸附率下降趋势不显著,对
Cd( Ⅱ ) 仍然有较高的 吸附能力 ,说明吸 附剂
PEI-SBC/Mt 具有良好的吸附再生性能。
图 11 PEI-SBC/Mt 结构示意图(a)及 PEI-SBC/Mt 吸附
Cd(Ⅱ)的机理图(b)
图 10 PEI-SBC/Mt 吸附剂的再生性能 Fig. 11 Schematic diagram of PEI-SBC/Mt structure (a) and
Fig. 10 Regeneration performance of PEI-SBC/Mt adsorbent mechanism of Cd(Ⅱ) adsorption by PEI-SBC/Mt (b)