Page 217 - 《精细化工》2023年第12期
P. 217
第 12 期 谢碧梅,等: 高活性 Cu-MnO 2 类氧化物纳米酶降解罗丹明 B ·2759·
30 ℃时,研究了 Cu-MnO 2 类氧化物酶对不同初始质 及降解中间产物会占据反应活性位点,导致降解率
量浓度(10~60 mg/L)RhB 的降解效果,结果见图 下降。与已有文献报道相比(表 3),Cu-MnO 2 类氧
7f。当 RhB 初始质量浓度为 50 mg/L 时,RhB 在 30 化物酶能催化溶解氧产生 ROS 用于快速降解 RhB,
min 内完全降解,而当 RhB 物质量浓度增至 60 无需额外氧化剂的协助,是一种绿色环保的污染物
mg/L,RhB 降解率下降,这可能是由于大量的 RhB 处理方法。
表 3 不同锰氧化物催化剂降解 RhB 的催化性能比较
Table 3 Comparison of catalytic performance of different manganese oxide catalysts for degradation of RhB
锰基氧化物催化降解 RhB 体系参数 参考
催化剂
催化剂质量浓度/(g/L) RhB 质量浓度/(mg/L) 条件 降解率/% 时间/min 文献
α-MnO 2 0.2 50 mL 5 mg/L pH=3.0 90 80 [33]
Mn 2CuO 4 0.2 50 mL 5 mg/L H 2O 2 (6 mmol/L) 96 45 [34]
MnO 2 0.5 10 mL 5 mg/L pH=2.5 97.6 10 [6]
CuO x/OMS 0.1 100 mL 20 mg/L PMS (0.83 mmol/L ) 98 180 [24]
MnO 2 0.1 250 mL 2.5 mg/L pH=3.0 99 10 [26]
MnO 2 0.1 50 mL 20 mg/L 0.25 g/L PMS,pH=3.3 99 12 [9]
Cu-MnO 2 0.1 100 mL 50 mg/L pH=3.0 100 30 本文
注:OMS 代表氧化锰八面体分子筛;PMS 代表过一硫酸盐。
此外,在 pH=3.0、温度为 30 ℃、RhB 水溶液质
量浓度为 30 mg/L 条件下,考察了浓度为 1 mmol/L 的
共存离子(NaCl、KCl、CaCl 2 、MgCl 2 、FeCl 3 、NaAc、
Na 2 CO 3 、NaNO 3 、Na 2 SO 4 、Na 2 HPO 4 )和质量浓度
为 10 mg/L 的腐植酸(HA)对 Cu-MnO 2 的催化降
解性能的影响,结果见图 8a。
3+
由图 8a 可见,在所有共存离子中,Fe 加入后对
类酶的催化性能影响最大,RhB 降解率下降了 10%,
3+
这可能是 Fe 与 Cu-MnO 2 发生氧化还原反应,削弱了
Cu-MnO 2 的氧化能力,进而影响其催化降解性能 [29] 。
由于 HA 会与 RhB 竞争材料表面的活性位点,甚至阻
塞材料的部分介孔通道,因此,HA 的加入会降低
Cu-MnO 2 催化降解 RhB 的效能 [35] 。循环使用实验(图
8b)结果表明,Cu-MnO 2 使用 5 次后 RhB 降解率降至
75%,可能是由于 Cu-MnO 2 催化剂表面浸出了少量金
属离子,以及污染物吸附在材料上覆盖了活性位点,
导致有效催化活性位点减少 [34-35] 。因此,可将Cu-MnO 2
负载在惰性载体上以提高循环稳定性。
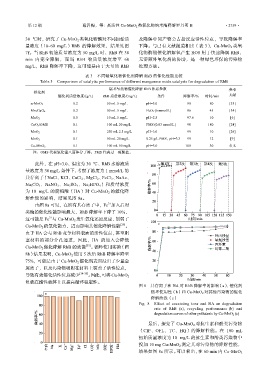
图 8 共存离子和 HA 对 RhB 降解率的影响(a)、催化剂
循环使用性(b)和 Cu-MnO 2 对其他污染物的催化
降解曲线(c)
Fig. 8 Effect of coexisting ions and HA on degradation
rate of RhB (a), recycling performance (b) and
degradation curves of other pollutants by Cu-MnO 2 (c)
最后,探究了 Cu-MnO 2 对抗生素和酚类污染物
(CIP、OFL、TC、HQ)的降解性能。在 100 mL
初始质量浓度为 10 mg/L 的抗生素和酚类污染物中
投加 10 mg Cu-MnO 2 测定其对污染物的降解性能,
结果如图 8c 所示。可以看出,在 60 min 内 Cu-MnO 2