Page 181 - 《精细化工》2023年第2期
P. 181
第 2 期 任龙芳,等: UiO-66-NH 2 /MoS 2 @PUF 的制备及其对 Cr(Ⅵ)的吸附 ·403·
2–
–
时,Cr 2 O 7 和 HCrO 4 起主导作用,酸性溶液中带正 60 min 时吸附容量达到了 100 mg/g,说明 Cr(Ⅵ)迅
2–
–
电的官能团和带负电的 Cr 2 O 7 和 HCrO 4 起强烈的静 速占据 UiO-66-NH 2 /MoS 2 @PUF 表面的吸附位点。
电相互吸引作用。按 1.3.10 节方法,考察了 pH 对 当吸附 时间 延至 70~240 min 时, UiO-66-NH 2/
UiO-66-NH 2 /MoS 2 @PUF 吸附性能的影响,结果见 MoS 2@PUF 的吸附速率较慢,原因可能是 Cr(Ⅵ)在
图 4b。由图 4b 可知,当 pH 在 2~4 时,Cr(Ⅵ)的去 吸附剂孔道扩散速度较慢。在 240 min 后基本达到
除率增加,在 pH 为 4 时去除率达到最大,达到 89%。 吸附平衡,吸附容量为 125 mg/g,这是由于当吸附
而当 pH 从 4 升高到 12 时,Cr(Ⅵ)的去除率又急剧 剂用量一定时,吸附剂位点被完全占据,达到吸附
+
下 降。当 溶液 中 H 浓度 较高时 , UiO-66-NH 2 / 平衡状态。如表 3 所示,与文献[31-33]相比,
+
MoS 2 @PUF 的表面趋于去质子化,随着 H 浓度降 UiO-66-NH 2 /MoS 2 @PUF 的平衡吸附容量明显优于
低,S 原子发生去质子化,活性位点增加 [31] ,所以在 其他材料。
pH 为 4 时,Cr(Ⅵ)的吸附容量达到最大。较高的 pH
会导致 UiO-66-NH 2 /MoS 2 @PUF 表面上带有更多的
负电荷,并且由于在其表面和离子之间强的静电排
斥而导致其吸附能力下降。在碱性条件下,过量的
–
OH 可能竞争 Cr(Ⅵ)的吸附活性位点,这是降低吸
附能力的另一个可能原因。由此可见,酸性条件有
利于吸附剂对 Cr(Ⅵ)的吸附,使 Cr(Ⅵ)与吸附剂表
面的正电荷高效快速地静电结合,吸附效果显著。
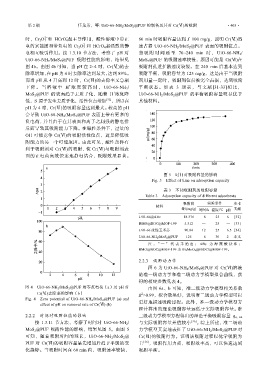
图 5 时间对吸附容量的影响
Fig. 5 Effect of time on adsorption capacity
表 3 不同吸附剂的吸附容量
Table 3 Adsorption capacity of different adsorbents
吸附容 实验条件 参考
材料
量/(mg/g) 时间/h 温度/℃ pH 文献
UiO-66@ABs 18.376 8 25 6 [32]
BMO@BOC@MOF-199 5.512 — 25 — [33]
UiO-66 改性玉米芯 90.04 12 25 6.5 [34]
UiO-66-NH 2/MoS 2@PUF 125 6 30 2 本文
注:“—”代 表未给出; ABs 为海藻酸盐珠;
BMO@BOC@MOF-199 为 Bi 2MoO 6@BiOCl@MOF-199。
2.2.3 吸附动力学
图 6 为 UiO-66-NH 2 /MoS 2 @PUF 对 Cr(Ⅵ)溶液
的准一级动力学和准二级动力学模型拟合曲线,获
得的相应参数见表 4。
图 4 UiO-66-NH 2 /MoS 2 @PUF 的零点电荷(a)及 pH 对 由图 6a、b 可知,准二级动力学模型相关系数
Cr(Ⅵ)去除率的影响(b) R >0.99,拟合效果好,说明准二级动力学模型可以
2
Fig. 4 Zero potential of UiO-66-NH 2 /MoS 2 @PUF (a) and
effect of pH on removal rate of Cr(Ⅵ) (b) 更好地描述吸附过程。此外,准一级动力学模型方
程计算出的理论吸附容量远低于实际吸附容量。准
2.2.2 时间对吸附性能的影响 二级动力学模型方程得出的理论平衡吸附容量 q e, cal
按 1.3.11 节方法,考察了时间对 UiO-66-NH 2 / 与实际吸附容量差值较小 [36] 。综上所述,准二级动
MoS 2 @PUF 吸附性能的影响,结果见图 5。由图 5 力学模型真实地表征了 UiO-66-NH 2 /MoS 2 @PUF 对
可知,随着吸附时间的延长,UiO-66-NH 2 /MoS 2 @ Cr(Ⅵ)的吸附行为。证明该吸附过程以化学吸附为
PUF 对 Cr(Ⅵ)的吸附容量呈先增加后趋于平缓的变 主 [36] ,吸附作用力强,吸附效率高,可以快速达到
化趋势。当吸附时间在 60 min 内,吸附速率较快, 吸附平衡。