Page 37 - 201810
P. 37
第 10 期 郭晓燕,等: 均一粒径 BaSO 4 微球的合成及产率 ·1645·
2+
显,反应-扩散协同调控机制 [19] 促进颗粒异向生长。 使 Ba 释放,生成新的 BaSO 4 ,产率得以提高。因
因此,BaSO 4 粒径分布变宽,粒径 0.8 μm 以下及 此,此方法适用于制备对粒径均一性要求不高的
2.0 μm 以上 BaSO 4 所占的比例均逐渐增加(图 5), BaSO 4 颗粒,可以有效提高产率。
形貌规整性及单分散性均逐渐下降。
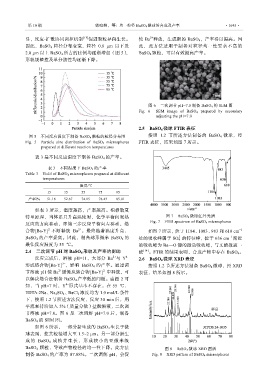
图 6 二次调节 pH=7.0 制备 BaSO 4 的 SEM 图
Fig. 6 SEM image of BaSO 4 prepared by secondary
adjusting the pH=7.0
2.5 BaSO 4 微球 FTIR 表征
图 5 不同反应温度下制备 BaSO 4 颗粒的粒径分布图 按照 1.2 节所述方法制备的 BaSO 4 微球,经
Fig. 5 Particle size distribution of BaSO 4 microspheres FTIR 表征,结果如图 7 所示。
prepared at different reaction temperatures
表 3 是不同反应温度下制备 BaSO 4 的产率。
表 3 不同温度下 BaSO 4 的产率
Table 3 Yield of BaSO 4 microspheres prepared at different
temperatures
温度/℃
15 35 55 75 95
76.43 85.01
产率/% 51.18 52.67 74.15
如表 3 所示,温度越高,产率越高。根据勒夏
特里原理,当体系只升高温度时,化学平衡向吸热 图 7 BaSO 4 微球红外光谱
Fig. 7 FTIR spectrum of BaSO 4 microspheres
反应的方向移动,即第三步反应平衡向左移动,络
2+
2
合物[Ba-Y] 不断释放 Ba 。最终随着温度升高, 如图 7 所示,位于 1184、1083、983 和 610 cm 1
2
1
BaSO 4 的产率提高。因此,制备球形微米 BaSO 4 的 处的吸收峰属于 SO 4 的特征峰,位于 636 cm 附近
最佳反应温度为 55 ℃。 的吸收峰为 Ba—O 键的振动吸收峰,与文献报道一
2.4 二次调节 pH 对 BaSO 4 形貌及产率的影响 致 [14] 。FTIR 的结果表明,合成产物中存在 BaSO 4 。
2+
反应完成后,溶液 pH=11,大部分 Ba 与 Y 4 2.6 BaSO 4 微球 XRD 表征
2
形成络合物[Ba-Y] ,影响 BaSO 4 的产率。通过调 按照 1.2 节所述方法制备 BaSO 4 微球,经 XRD
2
2+
节溶液 pH 使 Ba 缓慢从络合物[Ba-Y] 中释放,可 表征,结果如图 8 所示。
以解决络合法制备 BaSO 4 产率低的问题。由图 2 可
4
知,当 pH=7 时,Y 形式基本不存在。在 55 ℃、
EDTA2Na、Na 2 SO 4 、BaCl 2 浓度均为 1.0 mol/L 条件
下,按照 1.2 节所述方法反应,反应 30 min 后,用
平流泵持续加入 5%(质量分数)盐酸溶液,二次调
节溶液 pH=7.0。图 6 是二次调解 pH=7.0 后,制备
BaSO 4 的 SEM 图。
如图 6 所示,一部分新生成的 BaSO 4 生长于微
球表面,使其粒径增大至 1.5~2 μm。另一部分新生
成的 BaSO 4 成核并生长,形成较小的亚微米级
BaSO 4 颗粒,导致产物粒径的均一性下降。此方法 图 8 BaSO 4 微球 XRD 图谱
制备 BaSO 4 的产率为 87.88%。二次调解 pH,会促 Fig. 8 XRD pattern of BaSO 4 microspheres