Page 191 - 精细化工2020年第2期
P. 191
第 2 期 李文深,等: 乙酰胺基配位离子液体的合成及脱氮性能 ·393·
间 2 h、萃取温度 50 ℃的条件下,考察了 CH 3CONH 2
与 ZnCl 2 物质的量比对配位离子液体脱氮效果的影
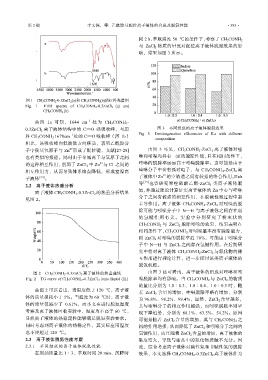
响,结果如图 3 所示。
图 1 CH 3 CONH 2 -0.3ZnCl 2 (a)和 CH 3 CONH 2 (b)的红外光谱图
Fig. 1 FTIR spectra of CH 3 CONH 2 -0.3ZnCl 2 (a) and
CH 3 CONH 2 (b)
由图 1a 可知,1644 cm –1 处为 CH 3 CONH 2 -
0.3ZnCl 2 离子液体结构中的 C==O 强吸收峰,与原 图 3 不同组成的离子液体脱氮效果
–1
料 CH 3 CONH 2 1670cm 处的 C==O 吸收峰(图 1b) Fig. 3 Denitrogenation efficiencies of ILs with different
composition
相比,该吸收峰向低波数方向移动,表明乙酰胺分
2+
子中羰基氧原子与 Zn 形成了配位键,文献[27-28] 由图 3 可见,CH 3 CONH 2 -ZnCl 2 离子液体对喹
也有类似的报道。同时由于金属离子与氧原子之间 啉和吲哚均具有一定的脱除性能,且在相同条件下,
–
2+
的这种相互作用,削弱了 ZnCl 2 中 Zn 与 Cl 之间的 喹啉的脱除率远远高于吲哚脱除率。这可能是由于
相互作用力,从而导致体系熔点降低,形成室温离 喹啉分子中含有孤对电子,与 CH 3 CONH 2 -ZnCl 2 离
2+
子液体 [24] 。 子液体中 Zn 的空轨道之间有较强的络合作用。Huh
等 [15] 也曾研究咪唑硫酸乙酯-ZnCl 2 类离子液体脱
2.2 离子液体热重分析
氮,并通过理论计算证实离子液体的 Zn 中心与喹啉
离子液体 CH 3 CONH 2 -0.3ZnCl 2 的热重分析结果
分子之间有较强的相互作用,在脱碱性氮过程中起
见图 2。
主导作用。离子液体 CH 3 CONH 2 -ZnCl 2 对吲哚的脱
除可能与吲哚分子中 N—H 与离子液体之间存在弱
的氢键作用有关。实验中分别研究了粉末状的
CH 3 CONH 2 与 ZnCl 2 脱除吲哚的效果,结果表明在
相同条件下,CH 3 CONH 2 对吲哚基本没有脱除能力,
而 ZnCl 2 对吲哚的脱除率近 70%,可能由于吲哚分
子中 N—H 与 ZnCl 2 之间存在氢键作用。在后期研
究中将对离子液体 CH 3 CONH 2 -ZnCl 2 与氮化物的相
互作用进行理论计算,进一步探讨该类离子液体的
脱氮机理。
图 2 CH 3 CONH 2 -0.3ZnCl 2 离子液体的热重曲线 由图 3 还可看出,离子液体的组成对喹啉和吲
Fig. 2 TG curve of CH 3 CONH 2 -0.3ZnCl 2 ionic liquid (IL) 哚脱除率均有影响。当 CH 3 CONH 2 与 ZnCl 2 的物质
的量比分别为 1.0∶0.3、1.0∶0.4、1.0∶0.5 时,随
由图 2 可以看出,当温度低于 120 ℃,离子液
着 ZnCl 2 含量的增加,喹啉脱除率略有增加,分别
体的质量损耗小于 5%;当温度为 60 ℃时,离子液 为 96.8%、98.2%、99.4%,显然,ZnCl 2 含量越多,
体的质量仅减少了 0.61%,而本文在进行脱氮温度 其与喹啉分子的相互作用越强;而吲哚脱除率则呈
考察及离子液体回收实验中,温度均不高于 60 ℃, 现下降趋势,分别为 68.1%、63.5%、54.2%。原因
显然离子液体的热稳定性能够满足脱氮实验要求。 可能是随着 ZnCl 2 含量的增加,其与 CH 3 CONH 2 之
同时考虑到离子液体的热稳定性,其实际应用温度 间的作用增强,从而降低了 ZnCl 2 和吲哚分子之间的
氢键作用,而且随着 ZnCl 2 含量的增加,离子液体的
也不应超过 120 ℃。
2.3 离子液体脱氮性能考察 黏度变大,导致与油品中的氮化物接触不充分。因
2.3.1 不同组成的离子液体脱氮性能 此,综合考虑离子液体对碱性氮和非碱性氮的脱除
在剂油质量比 1∶3、萃取时间 20 min、沉降时 效果,本文选择 CH 3 CONH 2 -0.3ZnCl 2 离子液体作为