Page 51 - 《精细化工》2020年第4期
P. 51
第 4 期 邢 杨,等: 富电子 LMOFs 对有机农药的高效荧光检测 ·685·
频率,而二者的差值(v)决定了羧基的配位方式。 随 TFL 加入量的增加逐渐降低。加入 0.40 μmol/L
–1
LMOF-1 和 LMOF-2 的v 分别为 180 和 206 cm , TFL 时,LMOF-1 及 LMOF-2 的荧光强度分别降低
说明羧酸根与 Zn(Ⅱ)的配位方式主要为单齿配位, 了 67.6%及 36.0%;加入 4.00 μmol/L TFL 时,
这一结果与文献[20]报道的结构相符。 LMOF-1 及 LMOF-2 的荧光几乎完全猝灭,荧光强
图 3c 为 LMOF-1 及 LMOF-2 的热失重曲线。由 度分别降低了 99.4%及 92.7%。
图 3c 可见,LMOF-1 在室温至 153 ℃范围内失重 图 5 分析了 LMOF-1 及 LMOF-2 荧光强度与
27.5%,归属于未配位的 H 2 O 及 DMF 分子;升温至 TFL 加入量的关系。
350 ℃后,LMOF-1 骨架迅速瓦解。LMOF-2 在室温
至 125 ℃范围内失重 3.24%,归属于 1.5 个未配位的
H 2 O 分子;升温至 395 ℃后,LMOF-2 骨架迅速瓦
解。以上分析说明,LMOF-1 及 LMOF-2 具有优异
的热稳定性。通过 PXRD 谱图及热失重曲线表明,
LMOF-2 孔道容纳客体分子的能力小于 LMOF-1。
2.2 有机农药的荧光检测
荧光探针与分析物的相互作用可改变前者的发
光强度。图 4 为 LMOF-1 及 LMOF-2 悬浊液加入 TFL
前后的荧光变化。
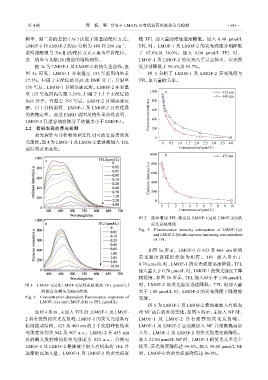
图 5 逐步增加 TFL 浓度后 LMOF-1(a)及 LMOF-2(b)的
荧光衰减曲线
Fig. 5 Fluorescence intensity attenuation of LMOF-1(a)
and LMOF-2 (b)with stepwise increasing concentrations
of TFL
如图 5a 所示,LMOF-1 在 423 及 460 nm 处的
荧光强度衰减趋势较为相符。TFL 加入量小于
0.70 μmol/L 时,LMOF-1 的荧光强度迅速降低;TFL
加入量大于 0.70 μmol/L 时,LMOF-1 的荧光强度下降
较缓慢。如图 5b 所示,TFL 加入量小于 1.00 μmol/L
图 4 LMOF-1(a)及 LMOF-2(b)对有机农药 TFL (μmol/L) 时,LMOF-2 的荧光强度迅速降低;TFL 的加入量
的浓度分辨荧光响应曲线 大于 1.00 μmol/L 时,LMOF-2 的荧光强度下降趋势
Fig. 4 Concentration-dependent fluorescence responses of 变缓。
LMOF-1(a) and LMOF-2(b) to TFL (μmol/L)
图 6 为 LMOF-1 及 LMOF-2 悬浊液加入有机农
如图 4 所示,未加入 TFL 时,LMOF-1 及 LMOF- 药 NF 前后的荧光变化。如图 6 所示,未加入 NF 时,
2 具有强烈的荧光发射峰;LMOF-1 的荧光光谱具有 LMOF-1 及 LMOF-2 具有强烈的荧光发射峰。
精细振动结构,423 及 460 nm 的 2 个发射峰初始荧 LMOF-1 及 LMOF-2 悬浊液加入 NF 并逐渐提高加
光强度分别为 942 及 907 a.u.;LMOF-2 在 453 nm 入量,LMOF-1 及 LMOF-2 的荧光强度逐渐降低。
处的最大发射峰初始荧光强度为 822 a.u.。分别向 加入 22.00 μmol/L NF 时,LMOF-1 的荧光几乎完全
LMOF-1 及 LMOF-2 悬浊液中加入有机农药 TFL 并 猝灭,荧光强度降低达 94.6%。加入 30.00 μmol/L NF
逐渐提高加入量,LMOF-1 及 LMOF-2 的荧光强度 时,LMOF-2 的荧光强度降低达 86.8%。