Page 27 - 《精细化工》2020年第6期
P. 27
第 6 期 王梦哲,等: 过渡金属硫化物在高级氧化法中的研究进展 ·1093·
2+
(反应 17、19)。Fe 与原位生成的 H 2 O 2 反应形成 的去除率仍可达到 98%。
大量的•OH,有效氧化有机污染物,在 1 h 内完全去 此外,将金属硫化物与 AC [75-76] 、MWCNTs [77]
除苯酚。5 次循环使用后,苯酚的去除率依旧接近 结合的复合材料应用于光催化或类 Fenton 反应来降
100%。该研究中 CdS/rGO 复合材料光催化反应 2 h 解污染物也表现出了优良的去除效果。
生成 580.68 μmol/L 的 H 2 O 2 ,且发现氧气的存在有 如表 2 所示,在 AOPs 中应用改性 TMS 对有机
助于反应的进行,这与 LIU [23] 、ZHOU [33] 、XIA [34] 、 污染物具有较强的去除能力。显然,这些工艺大多
•–
ZHU [45] 和 HAN [74] 等的研究结果类似。 是依靠•OH 或 SO 4 等自由基来降解污染物,而在实
– –
2•OH → H 2 O 2 (19) 际废水中含有大量的无机阴离子杂质(Cl 、HCO 3
–
HAN 等 [74] 制备的 CoMoS 2 -rGO 纳米片同样具 和 H 2 PO 4 等),自由基会与这些阴离子反应生成较弱
有原位生成 H 2 O 2 的作用,该研究对反应中的电子转 的自由基(Cl•、HCO 3 •和 H 2 PO 4 •等) [78-82] 。这种抑
移做了更深入的阐述:π 电子活化并从 rGO 转移到 制效果可能会降低实际废水中目标污染物的降解性
金属 Mo 和 Co 附近,由于 Mo 的电负性比 Co 大, 能。LUO 等 [83] 发现利用 N 掺杂石墨碳活化 PMS 时
•–
1
又导致电子分布呈现靠近 Mo 的趋势;在 RhB 降解 只产生了少量的自由基(•OH 或 SO 4 ),而 O 2 才是
过程中,溶液中的溶解氧在富电子的 Mo 中心附近 催化氧化过程中的主要反应物质。非自由基途径克
–
–
被还原为 HO 2 •/•O 2 ,HO 2 •/•O 2 进一步在 Co 中心附近 服了因自由基与阴离子之间的副反应引起的抑制作
–
被还原为 H 2 O 2 。最终,生成的 H 2 O 2 被活化生成•OH 用,而且催化过程中 Cl 转化成 HClO 更促进了催化
降解污染物。此外,污染物还可以充当电子供体在 效果。ZHANG 等 [84] 报道了 CuO 改善臭氧氧化作用
–
CoMoS 2 -rGO 纳米片的低电子区(rGO 附近)直接 而不会产生•OH,其中 HCO 3 (一种普遍存在的•OH
降解,从而促进了电子转移循环并维持电子得失平 清除剂)不仅没有抑制反应,反而显著增强了催化
衡。该工艺在降解 RhB 时的反应速率比传统的 性能。这为金属硫化物复合材料克服阴离子杂质的
Fenton 快大约 21 倍。经过 7 次循环使用后,RhB 抑制效果提出了新的研究方向。
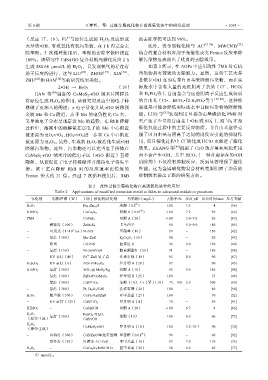
表 2 改性过渡金属硫化物在高级氧化法中的应用
Table 2 Applications of modified transition metal sulfides in advanced oxidation processes
氧化剂 光源/声源(W) (助)催化剂/活化剂 污染物/(mg/L) 去除率/% 反应 pH 反应时间/min 参考文献
①
H 2O 2 – F e 0.7Zn 0.3S 苯酚(0.2 ) 100 3.5 4 [56]
①
KHSO 5 – C u C o 2S 4 双酚 S(0.01 ) ~100 7.2 30 [62]
PMS – CuFeS 2 双酚 A(20) ~100 3.0~7.0 20 [63]
– 碘镓灯(100) Z n I n 2S 4 卡马西平 90 5.0~9.0 180 [85]
5
– 可见光(1×10 lux)N-ZnS 甲硝唑(10) 99 – 150 [42]
– 氙灯(300) M n - Z n S K 2Cr 2O 7(50) 90 – 20 [43]
– 阳光 C d - Z n S 茜素红 S 96 4.0 120 [44]
– 氙灯(150) Ni-ZnS/ZnO 靛蓝胭脂红(20) 91 – 180 [86]
– UV 汞灯(40) F e 3+ -ZnS 量子点 孔雀石绿(10) 95 8.0 90 [87]
K 2S 2O 8 U V 汞灯(6) ZnS-ZnFe 2O 4 罗丹明 B(20) 97 – 90 [45]
KHSO 5 氙灯(500) W O 3 @ MoS 2/Ag 双酚 A(10) 92 9.0 140 [88]
– 氙灯(500) B i F e W O 6/MoS 2 罗丹明 B(25) 100 – 75 [49]
– 氙灯(300) CdS/TiO 2 苯酚(10)、Cr(Ⅵ)(10) 73、100 2.0 300 [89]
– 氙灯(300) Pt, In 2O 3/CdS 孔雀石绿(20) 100 – 40 [90]
H 2O 2 超声波(100) C o F e 2O 4@ZnS 亚甲基蓝(25) 100 – 70 [52]
– UV 汞灯(125) CdS/TiO 2 罗丹明 B(4) 74 – 30 [91]
KHSO 5 – CoS@GN 双酚 A(20) ~100 6.7 8 [66]
H 2O 2 氙灯(300) FeSO 4·7H 2O、 苯酚(10) 100 6.0 60 [73]
(原位生成) CdS/rGO
H 2O 2 – CoMoS 2-rGO 罗丹明 B(10) 100 3.2~10.7 90 [74]
(原位生成)
①
– 卤钨灯(500) CdS/ZnO/氧化石墨烯 甲基橙(0.01 ) 99 – 60 [92]
– 紫外灯(150) N 掺杂 AC-ZnS 亚甲基蓝(10) 97 7.0 110 [75]
H 2O 2 – C u C o 2S 4/MWCNTs 亚甲基蓝(20) 98 6.0 20 [77]
① mmol/L。