Page 117 - 《精细化工》2020年第2期
P. 117
第 2 期 陈良哲,等: 水溶性碳量子点的制备及防伪应用 ·319·
率,计算公式如下:
m
/ % 100 (1)
m R
式中:φ 为 CQDs 的产率,%;m 为 CQDs 的质量,
mg;m R 为壳聚糖的质量,mg。
1.3.2 荧光量子产率计算
CQDs 的相对荧光量子产率采用参比法 [21] 获得,
通过与参照物(硫酸奎宁,0.1 mol/L 的 H 2 SO 4 为溶
剂,λ ex =366 nm,Q R =53%)的波长积分强度对比获
得,在测试过程中,样品溶液的光密度控制在
0.01~0.10,荧光量子产率(%)的计算公式如下:
I A n 2
Q Q R (2)
R
I R A n R 2
式中:Q 和 Q R 为 CQDs 和参照物的荧光量子产率,
%;I 和 I R 为 CQDs 和参照物综合荧光发射强度;A
和 A R 为 CQDs 和参照物吸光度;n 和 n R 为 CQDs
和参照物折射率(以水为溶剂时,均为 1.333)。
1.3.3 测试方法
FTIR 表征:采用溴化钾压片法,将 CQDs 粉末
与溴化钾研磨均匀后压制成透明薄片,设定波数范
–1
围为 4000~400 cm ,进行 FTIR 测试。
TEM 制样:将 CQDs 粉末超声分散在乙醇溶液
中,以 200 目的铜网为载体,捞取并在红外灯下干
燥后进行 TEM 测试。
XRD 表征:将 CQDs 粉末平铺于玻璃片的凹槽
中,设定角度范围为 2θ=10°~80°,进行 XRD 测试。
荧光表征:将 0.05 mg/L 的 CQDs 溶液置于
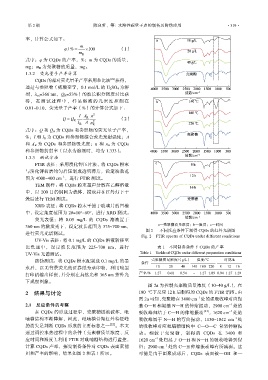
360 nm 的激发光下,设定波长范围为 375~700 nm, a—壳聚糖质量浓度;b—温度;c—时间
图 2 不同反应条件下制得 CQDs 的红外光谱图
进行荧光光谱测试。
Fig. 2 FTIR spectra of CQDs under different conditions
UV-Vis 表征:将 0.1 mg/L 的 CQDs 溶液转移至
比色皿中,设定波长范围为 225~700 nm,进行 表 1 不同制备条件下 CQDs 的产率
UV-Vis 光谱测试。 Table 1 Yields of CQDs under different preparation conditions
防伪测试:将 CQDs 粉末配制成 0.1 mg/L 的墨 条件 壳聚糖质量浓度/(g/L) 温度/℃ 时间/h
水后,以无背景荧光的证券纸为承印物,利用喷墨 10 20 40 140 180 220 8 12 16
打印机输出样张,并分别在自然光和 365 nm 紫外光 产率/% 1.27 0.68 0.54 – 1.27 1.09 0.94 1.27 1.29
下观察图像。
图 2a 为控制壳聚糖质量浓度(10~40 g/L),在
2 结果与讨论 180 ℃下反应 12 h 后制得的 CQDs 的 FTIR 谱图。由
–1
图 2a 可知,壳聚糖在 3400 cm 处的强吸收峰对应羟
2.1 反应条件的考察 基 O—H 和氨基 N—H 的伸缩振动,2900 cm 处的
–1
在 CQDs 的形成过程中,壳聚糖链被破坏,吡 吸收峰归结于 C—H 的伸缩振动 [23] ,1620 cm 处的
–1
喃糖结构不断降解,因此,吡喃糖骨架红外特征峰 吸收峰属于 N—H 的弯曲振动,1130~1042 cm 处
–1
的消失是判断 CQDs 形成的主要标志之一 [22] 。本文 的吸收峰对应吡喃糖结构中 C—O—C 骨架伸缩振
通过调控水热过程中的条件(壳聚糖质量浓度、反 动。 相较于壳聚糖,制得的 CQDs 在 3400 和
–1
应时间和温度),利用 FTIR 对吡喃糖结构进行监控, 1620 cm 处归属于 O—H 和 N—H 的吸收峰得到保
–1
计算 CQDs 产率,探究制备条件对 CQDs 表面官能 留;2900 cm 处的 C—H 伸缩振动峰有所减弱。这
团和产率的影响,结果如图 2 和表 1 所示。 可能是由于团聚成球后,CQDs 表面被—OH 和—