Page 182 - 《精细化工》2021年第8期
P. 182
·1676· 精细化工 FINE CHEMICALS 第 38 卷
内阻,有利于实现快速的电化学反应,从而提升材
料的倍率与循环性能 [20] 。利用四探针法 [21] 测定
LFMO-400、LFMO-450、LFMO-500 的电导率分别
为 0.00038、0.00030 和 0.00026 S/m,表明随着纳米
颗粒粒径的增大,材料的导电能力有所下降。
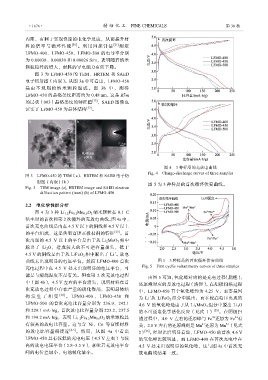
图 3 为 LFMO-450 的 TEM、HRTEM 和 SAED
电子衍射图(内嵌)。从图 3a 中可看出,LFMO-450
是由不规则的纳米颗粒组成。图 3b 中,测得
LFMO-450 的晶格条纹距离约为 0.48 nm,这是 R3¯m
的层状(003)晶格条纹的特征值 [12] ,SAED 图像也
证实了 LFMO-450 为晶体结构 [22] 。
图 4 3 种样品的充放电曲线
Fig. 4 Charge-discharge curves of three samples
图 3 LFMO-450 的 TEM(a)、HRTEM 和 SAED 电子衍
射图(内嵌)(b) 图 5 为 3 种样品的首次循环伏安曲线。
Fig. 3 TEM image (a), HRTEM image and SAED electron
diffraction pattern (inset) (b) of LFMO-450
2.2 电化学性能分析
图 4 为 3 种 Li 1.2 Fe 0.2 Mn 0.6 O 2 纳米颗粒在 0.1 C
倍率时的首次和第 2 次循环的充放电曲线。图 4a 中,
首次充电曲线是由在 4.5 V 以下的斜线和 4.5 V 以上
的平台组成,这是典型富锂正极材料的特征 [23] 。首
次出现的 4.5 V 以上的平台是由于从 Li 2 MnO 3 相中
脱出了 Li 2 O,造成较大的不可逆容量损失,低于
+
4.5 V 的斜线是由于从 LiFeO 2 相中脱出了 Li 。放电
曲线未出现明显的电压平台。然而 LFMO-400 首次 图 5 3 种样品的首次循环伏安曲线
充电过程中在 4.5 V 处未出现明显的电压平台,可 Fig. 5 First cyclic voltammetry curves of three simples
能是与煅烧温度不足有关。但在第 2 次充放电过程
由图 5 可知,氧化峰对应的是充电过程(脱锂),
中(图 4b),4.5 V 左右的平台消失,说明材料在首 还原峰对应的是放电过程(嵌锂)。在阳极扫描过程
次充放电过程中存在严重的极化作用,表明晶体结 中,LFMO-450 首个氧化峰约为 4.25 V,主要是因
构 发 生了相 变 [24] 。 LFMO-400 、 LFMO-450 和 为 Li 从 LiFeO 2 组分中脱出;而在较高电压出现的
+
LFMO-500 的首次充电比容量分别为 236.9、242.1 4.6 V 的氧化峰是由于从 Li 2 MnO 3 组分中脱出 Li 2 O
和 229.1 mA·h/g,首次放电比容量分别 223.2、237.5 的不可逆电化学活化反应(见式 1) [25] 。在阴极扫
和 199.2 mA·h/g,表明 Li 1.2 Fe 0.2 Mn 0.6 O 2 纳米颗粒具 描过程中,4.0 V 左右的还原峰与 Fe 还原为 Fe 有
4+
3+
有较高的放电比容量。这与含 Ni、Co 等富锂材料 关,2.8 V 左右的还原峰则是 Mn 还原为 Mn (见式
4+
3+
[26]
的放电比容量很接近 [4-5] 。然而,从图 4a 中看出 2) 。经对比后明显看出,LFMO-450 的首次 4.6 V
LFMO-450 具有较低的充电电压(4.5 V 左右)与较 的氧化峰比较明显,而 LFMO-400 在首次充电中在
高的放电电压平台(2.8~3.5 V),意味着充放电平台 4.5 V 处未出现明显的氧化峰,这与图 4a 中首次充
间的电位差最小,电池极化最小。 放电曲线结果一致。