Page 194 - 《精细化工》2022年第11期
P. 194
·2344· 精细化工 FINE CHEMICALS 第 39 卷
吸附 As(Ⅴ)后的 As 3d 谱见图 9b。图 9b 可观察到,
As 在约 45 eV 处出现特征峰,表明 As(Ⅴ)在
Fe 3 O 4 @surfactants 上有所吸附,3 种纳米颗粒对
As(Ⅴ)均有良好的吸附效果。
吸附 As(Ⅴ)前后 Fe 3O 4@surfactants 的 Fe 2p XPS
谱如图 10 所示。由图 10a 可知,Fe 3O 4@surfactants
在 710~724 eV 处的峰均属于 Fe 2p 轨道,且分别对
应于自旋轨道分裂产生的 Fe 2p 3/2 和 Fe 2p 1/2 。进一
步研究发现,在约 710 eV 处出现的拟合峰与 Fe 2+
的特征峰相符,结合能在约 713 和 724 eV 处的拟合 图 10 Fe 3 O 4 @surfactants 吸附 As(Ⅴ)前(a)、后(b)的
3+
峰为 Fe 的特征峰。此外,在结合能约为 718 eV 处 Fe 2p XPS 谱图
3+
出现的卫星峰归属于 Fe ,证明 Fe 以氧化态形式存 Fig. 10 Fe 2p XPS spectra of Fe 3 O 4 @surfactants before (a)
在 [40] 。如图 10b 所示,吸附 As(Ⅴ)后,Fe 2p 1/2 和 Fe and after (b) adsorption of As(Ⅴ)
2p 3/2 峰结合能降低,说明吸附作用使三价铁离子周 Fe 3 O 4 @surfactants 纳米颗粒吸附 As(Ⅴ)前后表
围的化学环境发生改变,从而使结合能发生了改变。 面电荷表征如图 11 所示。由图 11 可见,在未吸附
As(Ⅴ)的情况下,Fe 3 O 4 @surfactants 纳米颗粒的零
点电位均在 pH 7~8,pH<7 时,材料表面带正电,
pH>7 时,材料表面逐渐带负电。当其与 As(Ⅴ)接触
后,在整个 pH 范围内表面电荷均显著下降,可以
解释为 Fe 3 O 4@surfactants 与水相互作用过程中界面电
–
荷被修饰 [41] 。由于在水溶液中,As(Ⅴ)以 H 2 AsO 4 (pK a =
2–
3–
2.20)、HAsO 4 (pK a =6.97)和 AsO 4 (pK a =11.53)
–
等氧阴离子形式存在,在酸性至中环境下,H 2AsO 4
+
逐渐成为 As(Ⅴ)的主要形式,H 使 Fe 3O 4@surfactants
质子化程度升高,材料带正电,促使吸附效果提升;
但当 pH 升高至碱性时,Fe 3 O 4 @surfactants 与 As(Ⅴ)
–
之间的键合作用减弱,同时 OH 在 Fe 3O 4@surfactants
表面形成竞争吸附,使 As(Ⅴ)吸附在高 pH 范围内
不再占据主导,导致吸附能力下降 [42] 。
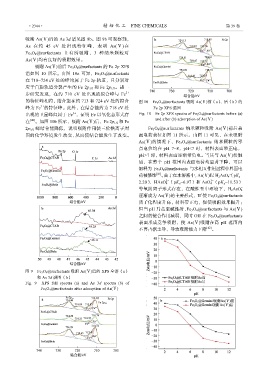
图 9 Fe 3 O 4 @surfactants 吸附 As(Ⅴ)后的 XPS 全谱(a)
和 As 3d 谱图(b)
Fig. 9 XPS full spectra (a) and As 3d spectra (b) of
Fe 3 O 4 @surfactants after adsorption of As(Ⅴ)