Page 105 - 《精细化工》2022年第12期
P. 105
第 12 期 刘耀鹏,等: 废弃花生壳活化热解炭用于检测芦丁的电化学传感 ·2471·
频率下的直线部分(对应于扩散过程) [31] 。如图 6
所示,PHAPC/GCE 的电子转移电阻最小,可能是
因为通过熔融盐活化热解后的炭材料中存在分级孔
隙结构,使电极与电解液接触的有效面积增加,电
子传输速率更快。
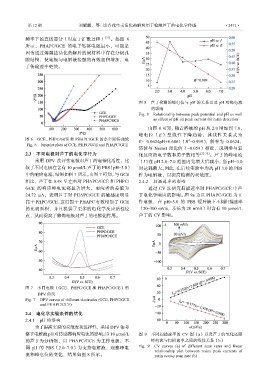
图 8 芦丁检测的峰电位与 pH 的关系以及 pH 对峰电流
的影响
Fig. 8 Relationship between peak potential and pH as well
as effect of pH on peak current for rutin detection
由图 8 可知,随着溶液的 pH 从 2.0 增加到 7.0,
峰电位(E)呈线性下降趋势,其线性关系式为
图 6 GCE、PHPC/GCE 和 PHAPC/GCE 的奈奎斯特曲线 E=–0.0624pH+0.6861(R =0.999),斜率为–0.0624,
2
Fig. 6 Nyquist plots of GCE, PHPC/GCE and PHAPC/GCE
该值与 Nernst 理论值(–0.059)相近,说明参与氧
2.3 不同电极对芦丁的电化学行为 化反应的电子数和质子数相等 [32-33] 。芦丁的峰电流
采用 DPV 法评估电极对芦丁的电催化活性,比 (I)在 pH 2.0~7.0 范围内先增大后减小,当 pH=3.0
较了不同电极在含有 10 µmol/L 芦丁的 PBS(pH=3.0) 时达到最大。因此,在后续实验中均选 pH 3.0 的 PBS
中的响应电流,结果如图 7 所示。由图 7 可知,与 GCE 作为电解液,以提高检测的灵敏度。
相比,芦丁在 0.48 V 左右对 PHAPC/GCE 和 PHPC/ 2.4.2 扫描速率的影响
GCE 的响应峰电流都显著增大,而两者的差值为 通过 CV 法研究扫描速率对 PHAPC/GCE 中芦
24.72 µA,表明芦丁对 PHAPC/GCE 的敏感度明显 丁电化学响应的影响。图 9a 为以 PHAPC/GCE 为工
高于 PHPC/GCE,这归因于 PHAPC 有效增加了 GCE 作电极,在 pH=3.0 的 PBS 缓冲液下不同扫描速率
的比表面积,并且提供了更多的电化学反应活性位 (20~300 mV/s,步长为 20 mV/s)对含有 10 µmol/L
点,从而提高了修饰电极对芦丁的电催化作用。 芦丁的 CV 影响。
图 7 不同电极(GCE、PHPC/GCE 和 PHAPC/GCE)的
DPV 曲线
Fig. 7 DPV curves of different electrodes (GCE, PHPC/GCE
and PHAPC/GCE)
2.4 电化学实验条件的优化
2.4.1 pH 的影响
为了提高实验的灵敏度和选择性,采用 DPV 法考
察了电解液pH 对传感器响应电流的影响。以10 µmol/L 图 9 不同扫描速率的 CV 图(a)以及芦丁的氧化还原
的芦丁为分析物,以 PHAPC/GCE 为工作电极,不 峰电流与扫描速率之间的线性关系(b)
同 pH 的 PBS(2.0~7.0)为支持电解液,观察峰电 Fig. 9 CV curves (a) of different scan rates and linear
relationship plot between redox peak currents of
流和峰电位的变化,结果如图 8 所示。 rutin versus scan rate (b)