Page 108 - 《精细化工》2019年第11期
P. 108
·2256· 精细化工 FINE CHEMICALS 第 36 卷
–1
–1
壳聚糖中 1600 cm 处的峰位移至 1636 cm ,并且
发生锐化,而海藻酸钠中—COO—对应的对称伸缩
–1
振动峰位由 1410 cm 移至 1429 cm –1[25] 。微胶囊分
–1
别保留了二甲酸钾在 1398 cm 处的—C==O 特征峰
和沸石分子筛大部分的特征峰,说明壳聚糖-海藻酸
钠形成的聚电解质膜将沸石分子筛和二甲酸钾包覆
在内。
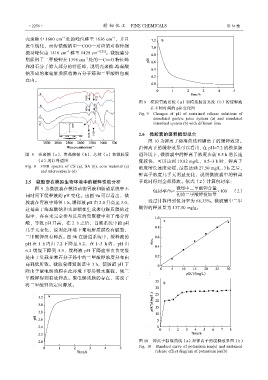
图 9 模拟胃液系统(a)和模拟肠道系统(b)的缓释液
在不同时间的 pH 变化图
Fig. 9 Changes of pH of sustained release solutions of
simulated gastric juice system (a) and simulated
intestinal system (b) with different time
2.6 微胶囊的缓释模型拟合
图 10 为钾离子标准曲线和钾离子的缓释效果。
由钾离子的缓释效果可以看出,在 pH=7.2 的模拟肠
图 8 壳聚糖(a)、海藻酸钠(b)、芯材(c)和微胶囊 道环境下,微胶囊中的钾离子浓度在前 0.5 h 增长速
(d)的红外谱图 度较快,可以达到 19.82 mg/L,0.5~3 h 时,钾离子
Fig. 8 FTIR spectra of CS (a), SA (b), core material (c) 浓度增长速度变缓,最高达到 27.50 mg/L,3 h 之后,
and microcapsule (d)
钾离子浓度几乎无明显变化,说明微胶囊中的钾离
2.5 微胶囊在模拟生物环境中的缓释性能分析 子此时得到全部释放。依式(2)计算包封率:
图 9 为微胶囊在模拟动物胃液和肠道系统中不 微球中二甲酸钾含量
包封率/%= 1 0 0 (2)
同时间下缓释液的 pH 变化。由图 9a 可以看出,微 初始二甲酸钾投加量
胶囊在胃液中滞留 1 h,缓释液 pH 由 2.0 升高至 3.0, 经过计算得到包封率为 68.33%,微胶囊中二甲
这是由于海藻酸钠和壳聚糖在生成聚电解质膜的过 酸钾的释放量为 137.50 mg/g。
程中,存在未完全参与反应的壳聚糖中和了部分胃
酸,导致 pH 升高,在 2 h 之后,胃液系统中的 pH
几乎无变化,说明此环境下聚电解质膜没有破裂,
二甲酸钾没有释放。图 9b 在肠道系统中,缓释液的
pH 在 1 h 内由 7.2 下降至 6.2,在 1~3 h 内,pH 由
6.2 缓慢下降到 5.9,缓释液 pH 下降速率由快变慢
是由于负载在沸石分子筛中的二甲酸钾浓度分布由
高到低所致。微胶囊滞留肠道中 3 h,使肠道 pH 下
降由于聚电解质膜在此环境下容易吸水胀破,使二
甲酸钾得到有效释放。聚电解质膜的存在,实现了
将二甲酸钾的定向释放。
图 10 钾离子标准曲线(a)和钾离子的缓释效果图(b)
Fig. 10 Standard curve of potassium ion(a) and sustained
release effect diagram of potassium ion(b)