Page 181 - 精细化工2019年第8期
P. 181
第 8 期 邓 斌,等: PDMDAAC 与一氯胺的反应动力学研究 ·1669·
和截 距,即曲线斜率为 0.9971,其截距 ln k 为 结合 2.1 节由测定一氯胺得到的反应速率常数
B
–5
B n
1.9402。其中, k k c A,0 。由此可得由反应物 B- k A 为 1.22×10 L/(mol·h),取其与 k B 平均值可以得
B
B
出 25 ℃下,PDMDAAC 与一氯胺反应生成 NDMA
PDMDAAC 测定得到的反应速率常数 k B 为 1.24×
–5
10 L/(mol·h)。 过程的初始阶段、PDMDAAC 开环降解反应的速率常
–5
数约为 1.23×10 L/(mol·h),总反应级数约为 1.9997,
对一氯胺和 PDMDAAC 分别为 1.0026 和 0.9971。
2.3 不同温度下反应速率常数的测定
为求得 PDMDAAC 与一氯胺反应生成 NDMA
过程的初始阶段、PDMDAAC 开环降解反应过程活
化能,实验参数测定中保持其他条件同 2.1 和 2.2 节
不变,仅分别改变温度为 15 和 35 ℃,进行相应温
度下,该开环降解反应速率常数的拟合计算,所得
实验结果如表 1 所示,表中 x、y 分别表示当采用初
始浓度法分别测定一氯胺和 PDMDAAC 的初始浓
度及其随时间变化规律时,得到的 lnc A,0、ln(dc A,0 /dt)
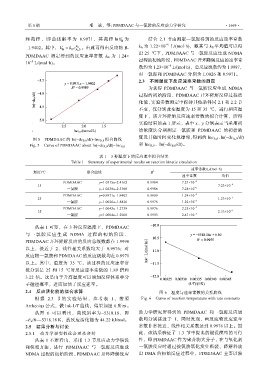
图 5 PDMDAAC 的 ln(dc B,0 /dt)lnc B,0 拟合曲线
和 lnc B,0、ln(dc B,0 /dt)。
Fig. 5 Curve of PDMDAAC about ln(dc B,0 /dt)lnc B,0
表 1 3 种温度下的反应速率拟合结果
Table 1 Summary of experimental results on reaction kinetic simulation
速率常数/L/(mol·h)
2
温度/℃ 拟合曲线 R
速率常数 均值
–6
PDMDAAC y=1.0315x–2.4162 0.9984 7.21×10
15 7.23×10
–6
–6
一氯胺 y=1.0230x–2.3368 0.9986 7.24×10
–5
PDMDAAC y=0.9971x–1.9402 0.9989 1.24×10
–5
25 1.23×10
–5
一氯胺 y=1.0026x–1.8826 0.9978 1.22×10
–5
PDMDAAC y=1.0043x–1.2739 0.9976 2.25×10
–5
35 2.33×10
–5
一氯胺 y=1.0004x–1.2900 0.9993 2.41×10
从表 1 可知,在 3 种反应温度下,PDMDAAC
与一氯 胺反 应生成 NDMA 过程的 初始阶 段、
PDMDAAC 开环降解反应的反应总级数都在 1.9998
以上,接近于 2,线性相关系数均大于 0.9976;对
反应物一氯胺和 PDMDAAC 的反应级数均在 0.9971
以上。其中,温度为 35 ℃,该过程的反应速率常
数分别是 25 和 15 ℃时反应速率常数的 1.89 倍和
3.22 倍。这是由于升高温度可以增加反应体系中分
子碰撞概率,进而加快了反应速率。
2.4 反应活化能的拟合求算 图 6 温度与速率常数的关系曲线
根据 2.3 节的 实验 结果, 参考 表 1,按照 Fig. 6 Curve of reaction temperature with rate constants
Arrhenius 公式,做 lnk-1/T 曲线,结果如图 6 所示。
从图 6 可以看出,曲线斜率为5318.18,即 动力学研究所得到的 PDMDAAC 和一氯胺反应级
E a /R=5318.18 K,故反应活化能为 44.22 kJ/mol。 数均分别接近于 1,同时发现,两反应物反应速率
2.5 结果分析与讨论 常数非常接近,线性相关系数达到 0.9976 以上。因
2.5.1 动力学模型假设合理性分析 此,该结果验证了 1.3 节中提出的假设模型的可行
从表 1 不难看出,采用 1.3 节反应动力学假设 性,即 PDMDAAC 作为聚合物大分子,在与氧化剂
和模型方法,进行 PDMDAAC 与一氯胺反应生成 一氯胺反应时通过被氯胺氧化发生断裂、降解释放
NDMA 过程的初始阶段、PDMDAAC 开环降解反应 出 DMA 的初始反应过程中,PDMDAAC 主要以独