Page 109 - 《精细化工》2021年第10期
P. 109
2+
第 10 期 孟宪娇: 基于 BODIPY 荧光探针对 Cu 和焦磷酸根的连续识别 ·2039·
2+
传感器Ⅰ对 Cu 和 PPi 是通过连续识别进行检测的。
与此同时,结合紫外和荧光谱图分析结果进一
2+
步对传感器Ⅰ同 Cu 和 PPi 可能的配位机理进行分
2+
析,见图 10。传感器Ⅰ在同 Cu 作用之前,测试溶
液于 516 nm 处呈现出较强的黄绿色荧光,当加入
2+
Cu 之后,荧光强度发生了明显的猝灭。当向配合
2+
2+
物Ⅰ-Cu 中加入 PPi 之后,PPi 将 Cu 从配位体系
中拉出来,使体系的荧光发生了恢复,恢复率可达
2+
到 98.5%。因此,传感器Ⅰ对 Cu 和 PPi 呈现出明
显的荧光“开-关”响应,而且最大发射波长也没有
发生明显的移动。另外,传感器分子本身为非共轭
体系,综合以上结论说明传感器Ⅰ的作用机理主要
是基于光诱导电子转移机理(PET 机理)进行识别
检测 [51-52] 。
2+
2.8 pH 对传感器Ⅰ检测 Cu 和 PPi 的影响
测试体系中的酸碱性往往会通过破坏传感器分
子本身的结构或者干扰配位方式,导致识别检测无
法实现。因此,为了探究传感器Ⅰ适用的 pH 范围,
室温下,在 pH 为 2~12 范围内测试传感器Ⅰ的荧光
强度变化,结果见图 11。如图 11 所示,当 pH 为 2~5
时,传感器Ⅰ的荧光强度会随着 pH 的增大而增大,
加入 PPi 后呈现出相同的变化趋势,所以在该范围
内进行响应测试时,pH 将成为干扰因素。当 pH 为
5~9 时,3 条曲线均呈现较平稳的趋势,这说明传感
器Ⅰ对 Cu 和 PPi 的响应在该 pH 范围内具有较好
2+
1
2+
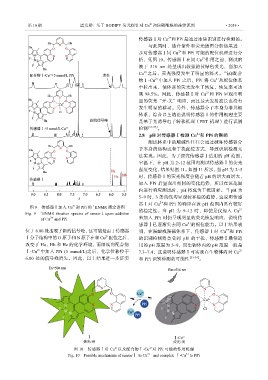
图 9 传感器Ⅰ加入 Cu 和 PPi 的 HNMR 滴定谱图 2+
1
Fig. 9 HNMR titration spectra of sensorⅠupon addition 的稳定性。当 pH 为 9~12 时,即使是仅加入 Cu
2+
of Cu and PPi 未加入 PPi 时仍呈现明显的荧光恢复响应,说明传
2+
感器Ⅰ已逐渐失去同 Cu 的配位能力。以上结果表
位于 6.00 处出现了新的信号峰,这可能是由于传感器 明,在强酸或强碱体系下,传感器Ⅰ对 Cu 和 PPi
2+
2+
Ⅰ分子结构中的 O 原子和 N 原子在和 Cu 配位之后, 的识别检测将会受到 pH 的干扰,传感器Ⅰ最佳适
改变了 Ha,Hb 和 Hc 的化学环境,而继续向配合物 用的 pH 范围为 5~9,而生物体内的 pH 范围一般是
2+
Ⅰ-Cu 中加入 PPi (5 mmol/L)之后,化学位移位于 7.3~7.4,这说明传感器Ⅰ可实现在生物体内对 Cu 2+
6.00 处的信号峰消失。因此,以上结果进一步证实 和 PPi 识别检测的可能性 [53-54] 。
2+
2+
图 10 传感器Ⅰ对 Cu 以及配合物Ⅰ-Cu 对 PPi 可能的作用机理
2+
Fig. 10 Possible mechanism of sensorⅠ to Cu 2+ and complex Ⅰ-Cu to PPi