Page 137 - 《精细化工》2022年第9期
P. 137
第 9 期 黄冬婷,等: 超声辅助离子液体提取人参多糖工艺及其抗氧化活性 ·1855·
2.1.4 超声时间对人参多糖提取量的影响
由图 1d 可知,人参多糖提取量随着超声时间增
加而增大。当超声时间为 30 min 时,人参多糖提取
量最大,此后随着超声时间的增加,提取量减小。
可能的原因是超声时间过长,人参多糖部分降解,
导致提取量降低 [25] 。因此,最佳超声时间为 30 min。
2.1.5 超声温度对人参多糖提取量的影响
由图 1e 可知,人参多糖的提取量随超声温度的
升高而大幅度增大。当温度为 70 或 80 ℃时,增幅
减小,此时,人参多糖提取量较高且相当。所以,
最终选择超声温度为 70 ℃。
2.2 正交实验及验证
根据上述单因素考察结果,对离子液体质量浓
度、料液比、超声时间和超声温度 4 个因素进行正
交实验优化。每个因素选择了 3 个水平,见表 1。
4
按照正交实验表 L9(3 )进行 9 组实验,结果见表 2。
表 1 正交实验的因素及水平
Table 1 Factors and levels of orthogonal experiment
A—1-乙基-3-甲基咪唑溴盐;B—1-丁基-3-甲基咪唑溴盐;C— 因素
1-己基-3-甲基咪唑溴盐;D—1-辛基-3-甲基咪唑溴盐
水平 A 离子液体 B 料液比/ C 超声 D 超声
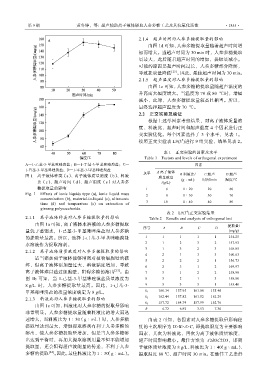
图 1 离子液体种类(a)、离子液体质量浓度(b)、料液 质量浓度
比(c)、超声时间(d)、超声温度(e)对人参多 /(g/L) (g∶mL) 时间/min 温度/℃
糖提取量的影响 1 6 1∶20 20 60
Fig. 1 Effects of ionic liquids type (a), ionic liquid mass 2 8 1∶30 30 70
concentration (b), material-to-liquid (c), ultrasonic
time (d) and temperature (e) on extraction of 3 10 1∶40 40 80
ginseng polysaccharide
4
表 2 L9(3 )正交实验结果
2.1.1 离子液体种类对人参多糖提取量的影响 Table 2 Results and analysis of orthogonal test
由图 1a 可知,离子液体水溶液的人参多糖提取
序号 A B C D 提取量/
量优于蒸馏水,1-己基-3-甲基咪唑溴盐对人参多糖 (mg/g)
的提取量最高。所以,选择 1-己基-3-甲基咪唑溴盐 1 1 1 1 1 154.25
2 1 2 3 2 157.93
水溶液作为提取溶剂。
3 1 3 2 3 168.85
2.1.2 离子液体质量浓度对人参多糖提取量的影响
4 2 1 3 3 160.63
适当添加离子液体能够增强对植物细胞壁的破
5 2 2 2 1 156.73
坏,但离子液体添加量过大,溶液黏度增加,导致 6 2 3 1 2 169.97
离子液体难以透过细胞壁,阻碍多糖的溶出 [23] 。由 7 3 1 2 2 158.98
图 1b 可知,当 1-己基-3-甲基咪唑溴盐质量浓度为 8 3 2 1 3 158.80
8 g/L 时,人参多糖提取量最高。因此,1-己基-3- 9 3 3 3 1 155.40
甲基咪唑溴盐的质量浓度确定为 8 g/L。 k 1 160.34 157.95 161.00 155.46
2.1.3 料液比对人参多糖提取量的影响 k 2 162.44 157.82 161.52 162.29
k 3 157.72 164.74 157.99 162.76
由图 1c 可知,料液比对人参多糖的提取量影响
R 4.72 6.92 3.53 7.30
非常明显。人参多糖提取量随着料液比的增大而迅
速增大,当料液比为 1∶30(g∶mL)时,人参多糖 由表 2 可知,各因素对人参多糖提取量影响程
提取量达到最大,增加提取溶剂有利于人参多糖的 度的主次顺序为 D>B>A>C,即提取温度为主要影响
溶出,使人参多糖提取量增加,但是当人参多糖溶 因素,其次为料液比,再次为离子液体质量浓度,
出达到平衡时,再加大提取溶剂用量不但不能增加 超声时间影响最小。最佳方案为 A2B3C2D3,即离
提取量,还会阻碍超声波能量的传递,不利于人参 子液体质量浓度为 8 g/L、料液比为 1∶40(g∶mL)、
多糖的提取 [24] 。因此,最佳料液比为 1∶30(g∶mL)。 提取温度 80 ℃、超声时间 30 min。在最佳工艺条件