Page 211 - 《精细化工》2023年第6期
P. 211
第 6 期 唐裕芳,等: 酚酸结构对酚酸-g-聚甘露糖醛酸抗氧化性能的影响 ·1361·
图 2D 显示了固定 PM (0.30 g),在 n(PM)∶ 2.3 PM-EDA 和 PA-g-PM 的表征
n(EDA)=1∶1.5,n(PM)∶n(EDC)∶n(NHS)=1∶2∶1 2.3.1 UV-Vis 吸收光谱分析
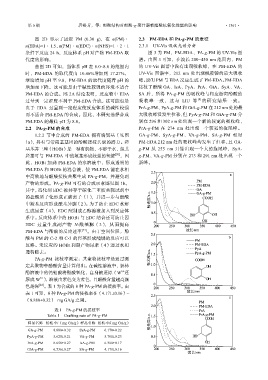
条件下反应 24 h,反应体系 pH 对产物 PM-EDA 取 图 3 为 PM、PM-EDA、PA-g-PM 的 UV-Vis 图
代度的影响。 谱。由图 3 可知,在波长 200~450 nm 范围内,PM
由图 2D 可知,当体系 pH 在 6.0~8.0 的范围内 的 UV-Vis 图谱中没有出现吸收峰,在 PM-EDA 的
时,PM-EDA 的取代度由 10.46%增加到 17.27%, UV-Vis 图谱中,212 nm 处出现酰胺键的最大吸收
继续增加 pH 至 9.0,PM-EDA 的取代度随着 pH 的 峰。说明 PM 与 EDA 反应生成了 PM-EDA。PM-EDA
增加而下降。这可能是由于碱性较强的环境不适合 接枝了酚酸 GA、IsA、PyA、PrA、GtA、SyA、VA、
PM-EDA 的合成。图 2A 结论表明,反应物中 EDA SA 后,所得 PA-g-PM 的吸收峰与相应游离酚酸的
过量到一定程度不利于 PM-EDA 合成,这可能也是 吸收峰一致,这与 LIU 等 [9] 的研究结果一致。
由于 EDA 过量到一定程度使反应体系的碱性较强 PrA-g-PM、PyA-g-PM 和 GtA-g-PM 在 212 nm 处的最
而不适合 PM-EDA 的合成。因此,本研究选择合成 大吸收峰没发生位移,但 PyA-g-PM 和 GtA-g-PM 分
PM-EDA 的最佳 pH 为 8.0。 别在 296 和 302 nm 处出现一个新的较宽的吸收峰,
2.2 PA-g-PM 的合成 PrA-g-PM 在 274 nm 处出现一个较宽的拖尾峰。
1.2.2 节中合成的 PM-EDA 拥有端氨基(见图 GA-g-PM、SyA-g-PM、VA-g-PM、SA-g-PM 相对
1a),具有与带羧基基团的酚酸接枝共聚的潜力。羟 PM-EDA 212 nm 处的吸收峰均发生了红移,且 GA-
基苯并三唑(HOBt)是一种有机物,不溶于水,但其 g-PM 从 255 nm 开始出现一个大的拖尾峰,SyA-
羟基可与 PM-EDA 中的氨基形成较强的氢键 [20] ,因 g-PM、VA-g-PM 分别在 273 和 291 nm 处出现一个
此,HOBt 加到 PM-EDA 的水溶液中,形成透明的 新峰。
PM-EDA 和 HOBt 的混合液,使 PM-EDA 能在水相
中高效地与酚酸接枝共聚生成 PA-g-PM,并避免副
产物的形成。PA-g-PM 可行的合成示意图见图 1b。
其中,活化剂 EDC 被共存于碳化二亚胺共轭试剂中
的盐酸质子化形成正碳离子(1),并进一步与酚酸
中羧基反应形成酰基异脲(2)。为了防止 EDC 水解
生成尿素(4),EDC 配制成乙醇溶液加入到反应体
系中。反应体系中的 HOBt 与 EDC 结合还可防止因
EDC 过量生成副产物 N-酰基脲(3),从而提高
PM-EDA 与酚酸的反应速率 [21] 。由于空间位阻,酚
酸与 PM 的 C-2 和 C-3 的羟基形成酯键的反应可以
忽略。未反应的 HOBt 和副产物尿素(4)通过水相
透析除去。
PA-g-PM 接枝率测定:共聚物接枝率是通过测
定共聚物中酚酸含量计算得出。在碱性溶液中,福林
6+
酚溶液中的钨钼酸将酚酸氧化,自身被还原(W 还
5+
原成 W ),溶液由紫色变为蓝色,且酚酸含量越高颜
色越深 [22] 。表 1 为合成的 8 种 PA-g-PM 的接枝率。由
表 1 可知,8 种 PA-g-PM 的接枝率在(4.171±0.16)~
(8.880±0.32) mg GA/g 之间。
表 1 PA-g-PM 的接枝率
Table 1 Grafting rate of PA-g-PM
样品名称 接枝率/ (mg GA/g) 样品名称 接枝率/(mg GA/g)
GA-g-PM 8.880±0.32 SyA-g-PM 6.170±0.22
PyA-g-PM 5.628±0.21 VA-g-PM 5.701±0.23
PrA-g-PM 8.658±0.27 IsA-g-PM 6.380±0.17
GtA-g-PM 6.536±0.27 SA-g-PM 4.171±0.16