Page 58 - 精细化工2019年第8期
P. 58
·1546· 精细化工 FINE CHEMICALS 第 36 卷
丁二醇结构中羟基上的氧能够提供孤对电子,在一 一类有机化学反应,本质上可以看作取代,是具有
定温度和催化剂条件下主动去进攻正电性较强的富 两个或两个以上官能团的单体,相互反应生成高分
马酸二乙酯结构中羰基碳正离子,亲核加成消去乙 子化合物,同时产生有简单分子(醇)的化学反应。
醇分子,即通过酯交换反应得到中间产物。同时可 兼有缩合出低分子和聚合成高分子的双重含义,反
以从反应装置末端收集到一定量的副产物乙醇,通 应产物称为缩聚物。通常缩聚反应的可逆程度由平
过监测乙醇的量能够判断酯交换反应进行的程度。 衡常数来确定,聚合物酯化反应的平衡常数较小,
第一步反应中加入氯化锌为催化剂,对苯二酚为阻 低分子副产物醇的存在限制了相对分子质量的提
聚剂,其中对苯二酚可以同反应体系中的自由基作 高,需要在高度减压条件下脱除,故在反应过程中
用,可能形成非自由基物质,或形成活性较低、不 需要将体系中生成的醇及时排出,这样有利于反应
能够再引发的自由基,这样可以有效阻止富马酸二 向生成聚合物 PBF 的方向进行。因此,需要在实验
乙酯分子内双键之间发生反应。第二步缩聚反应是 中保持反应体系的真空度为 670 Pa 左右。
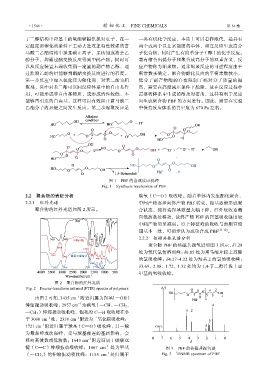
图 1 PBF 的合成反应机理
Fig. 1 Synthesis mechanism of PBF
2.2 聚合物的表征分析 碳氧(C—O)吸收峰。随着单体内发生酯化聚合,
2.2.1 红外光谱 中间产物逐步向终产物 PBF 转变,羟基逐渐形成聚
聚合物的红外光谱如图 2 所示。 合状态,使得端羟基数量大幅下降,红外吸收逐渐
向低波数处移动,故终产物 PBF 的羟基吸收强度较
中间产物明显减弱。以上特征峰的吸收与预期官能
团基本一致,可初步认为成功合成 PBF [11-12] 。
2.2.2 核磁共振氢谱分析
聚合物 PBF 的核磁共振氢谱如图 3 所示,δ7.28
处为氘代氯仿溶剂峰;δ6.85 处为富马酸片段上双键
的氢吸收峰;δ4.27~4.22 处为羟基上的氢的吸收峰;
δ3.69、2.08、1.72、1.32 处均为 1,4-丁二醇片段上亚
甲基的氢吸收峰。
图 2 聚合物的红外光谱
Fig. 2 Fourier-transform infrared (FTIR) spectra of polymers
–1
由图 2 可知,3435 cm 附近归属为羟基(—OH)
–1
伸缩振动吸收峰;2957 cm 为碳氢(—CH、—CH 2 、
—CH 3 )伸缩振动吸收峰,饱和的 C—H 吸收峰在小
–1
–1
于 3000 cm 处;2358 cm 附近为二氧化碳吸收峰;
–1
1721 cm 附近归属于羰基(C==O)吸收峰,其一般
为最强峰或次强峰,受与羰基相连的基团影响,会
–1
移向高波数或低波数;1643 cm 附近归属于碳碳双
键(C==C)伸缩振动吸收峰;1467 cm –1 处为甲基 图 3 PBF 的核磁共振氢谱
1
–1
(—CH 3 )的伸缩振动吸收峰;1155 cm 处归属于 Fig. 3 HNMR spectrum of PBF