Page 158 - 《精细化工》2023年第12期
P. 158
·2700· 精细化工 FINE CHEMICALS 第 40 卷
该基团末端的羟基作为氢键供体与底物 DMC 的羰 TEPA-EC 与 EtOH 混合物中—OH 的振动吸收峰出
–1
基氧原子形成氢键,使羰基碳原子的正电荷密度增 现在为 3338 cm 处,相对于 EtOH 中的—OH 振动
–1
加,提高了 DMC 羰基的亲电性,这种协同氢键作 吸收峰(3310 cm )发生了蓝移、相对于 TEPA-EC
–1
用使 EtOH 以较低的活化能进攻 DMC,生成含羟基 中的—OH 振动吸收峰(3352 cm )发生了红移。
–1
的原酸酯;(2)原酸酯不稳定,分解为 EMC 和 DMC 中的 C==O 在 1750 cm 处产生强吸收,与
MeOH;(3)DMC、EtOH 分别从催化剂的活性位点 TEPA-EC 混合后,DMC 中的 C==O 在该处的吸收峰
上置换出 EMC 和 MeOH,形成催化循环。 强度明显减弱、并与 TEPA-EC 中的 C==O 的伸缩振
–1
在上述反应历程中,EtOH 分子必须以氢键供体 动吸收峰合并后,整体红移至 1672 cm 处;混合物
的形式与催化剂中的氢键受体形成氢键才有可能被 中 TEPA-EC 的—OH 的伸缩振动吸收峰则从混合前
–1
–1
活化。多元胺与 EC 反应产物中的仲胺基甲酸羟乙 3352 cm 红移至 3311 cm 。结果表明,TEPA-EC
基酯中的仲胺氮原子,虽然也能以受体的形式与 与 EtOH、DMC 之间存在强烈的氢键作用 [25-26] 。
EtOH 供体分子形成氢键,但其碱性较叔胺氮原子
低、供电子能力较弱,对 EtOH 分子的活化程度有
限。此外,与仲胺氮原子相连的氢原子也可作为供
体与作为受体的 EtOH 分子形成氢键,该氢键对
EtOH 无活化作用,反而会降低 EtOH 的亲核性。仲
胺基甲酸羟乙酯末端的醇羟基还有可能以“咬尾”
的方式形成分子内氢键,从而失去活化 DMC、EtOH
分子的能力。综上,仲胺基甲酸羟乙酯基团对酯交
换无催化活性。在 EC 与各多元胺所含氨基等物质
的量反应的条件下,DETA-EC、TETA-EC 中叔胺基
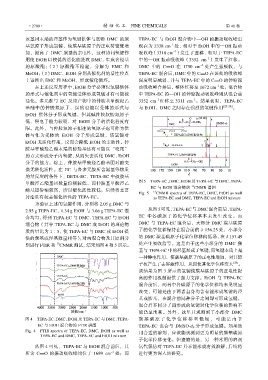
甲酸羟乙酯基团数量份额较低、而仲胺基甲酸羟乙 图 5 TEPA-EC、DMC、EtOH 及 TEPA-EC 与 DMC、TEPA-
EC 与 EtOH 混合物的 13 CNMR 谱图
酯基团份额较高,所以催化活性较低;后续将主要
Fig. 5 13 CNMR spectra of TEPA-EC, DMC, EtOH as well
讨论具有较高催化活性的 TEPA-EC。 as TEPA-EC and DMC, TEPA-EC and EtOH mixture
为验证上述的氢键作用,分别将 2.05 g DMC 与
2.95 g TEPA-EC、1.34 g EtOH 与 3.66 g TEPA-EC 混 从图 5 可见,TEPA-EC 与 DMC 混合前后,TEPA-
合均匀,得到 TEPA-EC 与 DMC、TEPA-EC 与 EtOH EC 中各碳原子的化学位移基本未发生改变。而
混合物(其中 TEPA-EC 与 DMC 或 EtOH 的理论物 DMC 与 TEPA-EC 混合后,大部分 DMC 羰基碳原
质的量比为 1∶5,使 TEPA-EC 与 DMC 或 EtOH 提 子的化学位移保持在混合前的 δ 156.25 处,小部分
供的羰基或羟基数量相等);对两混合物及其原料分 的 DMC 羰基碳原子化学位移移向低场,在 δ 157.49
13
别进行 FTIR 和 CNMR 测试,结果如图 4 和 5 所示。 处产生吸收信号。这是由于这些小部分的 DMC 羰
基与 TEPA-EC 中的羟基形成了氢键,而氢键本质上是
一种静电作用,使碳基碳原子的正电性增加,对其原
子核产生了去屏蔽作用,从而使其化学位移变大 [26] 。
该结果为图 3 所示的氢键使羰基碳原子的正电性提
高的作用机制提供了强力支撑。EtOH 与 TEPA-EC
混合前后,两者中各碳原子的化学位移均未见明显
改变,可能是由于两者自身均含有能形成氢键的羟
基或胺基,在混合前同种分子之间即可形成氢键,
混合后不同分子间形成的氢键对化学位移的影响不
能凸显出来。另外,这里只观测到了小部分 DMC
图 4 TEPA-EC、DMC、EtOH 及 TEPA-EC 与 DMC、TEPA- 羰 基碳原 子化 学位移 移至 低场, 可能 是由 于
EC 与 EtOH 混合物的 FTIR 谱图 TEPA-EC 也会与 DMSO-d 6 分子形成氢键。如果选
Fig. 4 FTIR spectra of TEPA-EC, DMC, EtOH as well as 用合适的溶剂,应该能观测到更为明显的羰基碳原
TEPA-EC and DMC, TEPA-EC and EtOH mixture
子化学位移变化。但遗憾的是,另一种常用的溶剂
从图 4 可见,TEPA-EC 与 EtOH 混合前后,其 氘代氯仿对 TEPA-EC 并不能形成有效溶解,后续将
–1
所含 C==O 的振动吸收峰均位于 1699 cm 处;而 进行更为深入的研究。