Page 145 - 201811
P. 145
第 11 期 余 跃,等: 催化剂对双氧水氧化淀粉-锆配合物结构及鞣制性能的影响 ·1931·
表 1 催化剂类型对淀粉氧化度的影响
Table 1 Effect of catalyst type on the oxidation degree of
starch
对照 WO 4 VO 3 Fe Cu Cu-Fe
氧化度/% 8.9 15.0 38.7 61.5 64.1 72.5
a—对照;b—WO 4;c—VO 3;d—Fe;e—Cu;f—Cu-Fe
图 1 催化剂类型对双氧水分解率的影响
Fig. 1 Effect of catalyst type on the decomposition rate of
hydrogen peroxide
2.2 催化剂类型对氧化淀粉化学结构的影响
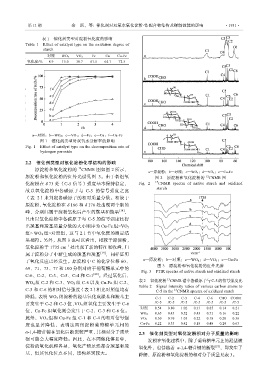
原淀粉和氧化淀粉的 13 CNMR 图如图 2 所示,
a—原淀粉;b—对照;c—WO 4;d—VO 3;e—Cu-Fe
原淀粉和氧化淀粉的红外光谱见图 3。由于各组氧 图 2 原淀粉和氧化淀粉的 13 CNMR 图
化淀粉在δ73 处(C-5 信号)强度基本保持稳定, Fig. 2 13 CNMR spectra of native starch and oxidized
starch
故以氧化淀粉中各碳原子与 C-5 的信号强度之比
(表 2)来判定各碳原子的相对质量分数。相较于
原淀粉,氧化淀粉在δ166 和δ176 处出现两个新的
峰,分别归属于淀粉氧化后产生的羰基和羧基 [18] ,
且由以氧化淀粉中各碳原子与 C-5 的信号强度比得
出羰基和羧基质量分数的大小顺序为 Cu-Fe 组>VO 3
组> WO 4 组>对照组,这与 2.1 节中氧化度的测定结
果相符。另外,从图 3 也可以看出,相较于原淀粉,
1
氧化淀粉于 1735 cm 处出现了新的特征吸收峰,归
属于淀粉分子中新生成的羰基和羧基 [19] ,同样证明
了氧化反应已经发生。原淀粉中 C 的化学位移 60、 a—原淀粉;b—对照;c—WO 4 ;d—VO 3 ;e—Cu-Fe
图 3 原淀粉和氧化淀粉的红外光谱
69、71、73、77 和 100 分别对应于葡萄糖单元中的 Fig. 3 FTIR spectra of native starch and oxidized starch
C-6、C-2、C-3、C-5、C-4 和 C-1 [20] 。经过氧化后,
13
WO 4 组 C-2 和 C-3、VO 3 组 C-6 以及 Cu-Fe 组 C-2、 表 2 氧化淀粉 CNMR 谱中各碳原子与 C-5 的信号强度比
Table 2 Signal intensity ratios of various carbon atoms to
C-3 和 C-6 的相对信号强度(表 2)相比对照组均有 C-5 in the CNMR spectra of oxidized starch
13
降低,表明 WO 4 组淀粉的羟基氧化成羰基和羧基主 C-1 C-2 C-3 C-4 C-6 CHO COOH
要发生于 C-2 和 C-3 位,VO 3 组氧化主要发生于 C-6 /C-5 /C-5 /C-5 /C-5 /C-5 /C-5 /C-5
对照 0.54 0.80 1.02 0.33 0.65 0.14 0.21
位,Cu-Fe 组氧化则会发生于 C-2、C-3 和 C-6 位。
WO 4 0.65 0.43 0.52 0.43 0.71 0.16 0.22
此外,VO 3 组和 Cu-Fe 组 C-1 和 C-4 的相对信号强 VO 3 0.30 0.76 1.03 0.22 0.18 0.20 0.36
度也显著降低,表明这两组淀粉葡萄糖单元间的 Cu-Fe 0.22 0.33 0.42 0.18 0.48 0.29 0.63
α-1,4-糖苷键在氧化后断裂较严重,其相对分子质量 2.3 催化剂类型对氧化淀粉相对分子质量的影响
很可能会大幅度降低。因此,在不同催化体系中, 淀粉在氧化过程中,除了葡萄糖单元上的羟基被
淀粉的氧化机理各异,氧化产物虽然都含羰基和羧 氧化外,也伴随着 α-1,4-糖苷键的断裂 [21] ,即发生了
基,但其氧化位点不同,结构差别较大。 降解,原淀粉和氧化淀粉的相对分子质量见表 3。