Page 76 - 《精细化工》2020年第9期
P. 76
·1790· 精细化工 FINE CHEMICALS 第 37 卷
色的强荧光(图 1a)。当往 TM 的乙腈溶液中加入
0.5 倍物质的量 Cu(Ⅱ)(图 1c 中),溶液虽立即变为
肉红色,但几乎无荧光(图 1d 中);当往 TM 的乙
腈溶液中加入 5 倍物质的量 Cu(Ⅱ)(图 1c 右),溶
液颜色较之前虽变淡,为淡肉红色,但显示出明显
的蓝色荧光(图 1d 右);通过往 TM 的乙腈溶液中
加水,随着水含量的逐渐增多,荧光强度显著增强,
说明溶液中产生了聚集态分子,TM 表现出了聚集
荧光增强的特性。通过查阅文献发现,C==N 基团中
的 N 和邻近的酚羟基易形成分子内氢键 [15] (图 1b)。
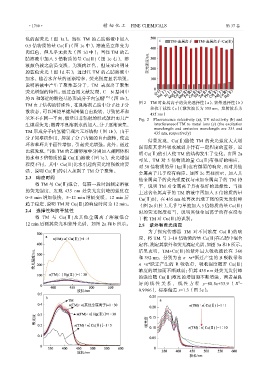
图 2 TM 对金属离子的荧光选择性(a)、紫外选择性(b)
TM 由于结构的特殊性,在良溶剂乙腈中分子处于分
和抗干扰性(c)(激发波长为 355 nm,发射波长为
散状态,可以围绕单键周围做自由旋转,导致芘环和 435 nm)
苯环不在同一平面,能量以非辐射的形式散出而只产 Fig. 2 Fluorescence selectivity (a), UV selectivity (b) and
生微弱荧光;随着不良溶剂水的加入,分子逐渐聚集, interferenceof TM to metal ions (c) (the excitation
wavelength and emission wavelength are 355 and
TM 形成分子内氢键呈现六元环结构(图 1b),由于 435 nm, respectively)
分子间堆积作用,抑制了分子内键的自由旋转,使芘
结果发现,Cu(Ⅱ)能使 TM 的荧光强度大大增
环和苯环共平面性增加,引起荧光增强。此外,通过 强而使其紫外吸收减弱并伴有一定程度的蓝移,说
比较发现,当往 TM 的乙腈溶液中分别加入相同体积
明 Cu(Ⅱ)的引入使 TM 的结构发生了变化。由图 2a
的水和 5 倍物质的量 Cu(Ⅱ)溶液(图 1e),荧光增强
可见,TM 对 5 倍物质的量 Cu(Ⅱ)有很好的响应,
程度不同,其中 Cu(Ⅱ)比水引起的荧光增强效应要 对 30 倍物质的量 Hg(Ⅱ)也有微弱的响应,而对其他
强,说明 Cu(Ⅱ)的引入加剧了 TM 分子聚集。
金属离子几乎没有响应。如图 2c 黑柱所示,加入其
2.3 响应时间
他金属离子的荧光强度仅与未加金属离子的 TM 持
将 TM 与 Cu(Ⅱ)混合,每隔一段时间测定溶液 平,说明 TM 对金属离子具有很好的选择性。当往
的荧光强度,发现 435 nm 处荧光发射峰的强度在 上述含金属离子的 TM 溶液中再加入 5 倍物质的量
0~5 min 增加很快,5~12 min 增幅变缓,12 min 后 Cu(Ⅱ)时,在 435 nm 处再次出现了强的荧光发射峰
趋于稳定,说明 TM 对 Cu(Ⅱ)的响应时间为 12 min。 (图 2c 红柱),几乎与单独加入 5 倍物质的量 Cu(Ⅱ)
2.4 选择性和抗干扰性 时的荧光强度相当,说明其他金属离子的存在没有
将 TM 与 Cu(Ⅱ)及其他金属离子溶液混合 干扰 TM 对 Cu(Ⅱ)的识别。
12 min 后测其荧光和紫外光谱,如图 2a 和 b 所示。 2.5 紫外和荧光滴定
为了探究传感器 TM 对不同浓度 Cu(Ⅱ)的响
应,将 TM 与 1~10 倍物质的量 Cu(Ⅱ)在乙腈中混合
定容,测定其紫外和荧光滴定光谱,如图 3a 和 b 所示。
结果表明,TM+Cu(Ⅱ)的紫外最大吸收波长在 360
和 392 nm,分别为由 π→π*跃迁产生的 B 吸收带和
n→π*跃迁产生的 R 吸收带,吸收强度随着 Cu(Ⅱ)
浓度的增加而不断减弱;但其 435 nm 处荧光发射峰
的强度随 Cu(Ⅱ)浓度的增加而不断增强,两者呈良
2
好的线性 关系,线 性方程 y=80.5x+33.9 ( R =
0.9966),标准偏差 s=1.3(图 3c)。