Page 174 - 《精细化工》2021年第12期
P. 174
·2536· 精细化工 FINE CHEMICALS 第 38 卷
脱水成环生成 N-苄基-5-甲基-2-吡咯烷酮。除此之
外还检测到副产物 5-甲基-2-吡咯烷酮。值得注意
的是,在反应 6 h 时,N-苄基-5-甲基-2-吡咯烷酮
的收率达到了最大,为 95.0%,说明催化剂 5% Pd/
10% CeO 2 -Al 2 O 3 在催化乙酰丙酸与苄胺还原胺化
反应中具有很好的催化活性和优异的 N-苄基-5-甲
基-2-吡咯烷酮选择性。结合图 5 和 6 综合分析,
乙酰丙酸与苄胺还原胺化仅 1 h 乙酰丙酸能完全
转化,而苯甲腈的加氢反应需 3 h 才能完全转化。
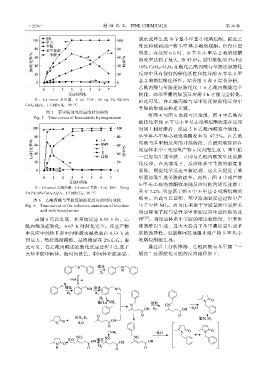
注:4.8 mmol 苯甲腈、5 mL THF、30 mg 5% Pd/10% 由此可见,在乙酰丙酸与苯甲腈还原胺化反应中
CeO 2-Al 2O 3、1.5 MPa H 2、90 ℃
苄胺的形成是控速步骤。
图 5 苯甲腈加氢反应的时间曲线
Fig. 5 Time curves of benzonitrile hydrogenation 将图 4 与图 6 比较可以发现,图 4 中乙酰丙
酸转化率和 N-苄基-5-甲基-2-吡咯烷酮收率在反应
时间上相对滞后,反应 5 h 乙酰丙酸完全转化,
N-苄基-5-甲基-2-吡咯烷酮收率为 87.5%。在乙酰
丙酸与苯甲腈反应的开始阶段,乙酰丙酸保留在
反应体系中(无加氢产物 γ-戊内酯生成),苯甲腈
一旦加氢生成苄胺,立即与乙酰丙酸发生还原胺
化反应。在此情况下,反应体系中苄胺的浓度非
常低,根据化学反应平衡原理,这大大促进了苯
甲腈加氢生成苄胺的速率。此外,图 4 中副产物
5-甲基-2-吡咯烷酮收率随反应时间的延长逐渐上
注:4.0 mmol 乙酰丙酸、4.8 mmol 苄胺、5 mL THF、30 mg
5% Pd/10% CeO 2-Al 2O 3、1.5 MPa H 2、90 ℃ 升至 7.2%,明显高于图 6 中 5-甲基-2-吡咯烷酮的
收率。由此可以证明,苯甲腈加氢反应过程中产
图 6 乙酰丙酸与苄胺还原胺化反应的时间曲线
Fig. 6 Time curves of the reductive amination of levulinic 生了少量 NH 3 。而 NH 3 来源于苄胺氢解生成甲苯
acid with benzylamine 的过程和苄胺与活性苯甲亚胺反应生成仲胺的过
由图 6 可以发现,在开始反应 0.33 h 内,乙 程 [28] 。当反应体系中苄胺的浓度较低时,甲苯和
酰丙酸迅速转化,0.67 h 时转化完全。反应产物 仲胺难以生成,这大大提高了苯甲腈加氢生成苄
中反应中间体Ⅱ和中间体席夫碱收率在 0.33 h 达 胺的选择性,也能够间接地阻止副产物 5-甲基-2-
到最大,然后逐渐降低,最终稳定在 2%左右。由 吡咯烷酮的生成。
此可见,在乙酰丙酸还原胺化反应过程中生成了 通过以上分析推测,乙酰丙酸与苯甲腈“一
大量亚胺中间体,随时间延长,中间体亚胺加氢、 锅法”还原胺化可能的反应路径如下: