Page 32 - 《精细化工》2022年第10期
P. 32
·1966· 精细化工 FINE CHEMICALS 第 39 卷
如图 1 所示,解耦转移机制分为质子转移(PT) 1.2 质量传输
和电子转移(ET)两类反应,且二者可以单独作用, 催化反应由表面反应和传质两部分组成。当传
协同转移机制则是在同一个反应步骤中同时涉及到 质通量明显慢于表面反应速率时,动力学不再是影
协同质子-电子转移(CPET)。HER 的 CPET 路径如 响反应速率的主要因素,此时,系统性能很大程度
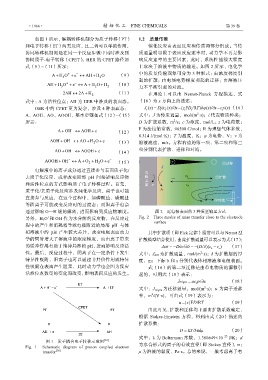
式(9)~(11)所示: 上取决于溶液中物质的输送。如图 2 所示,电化学
AH O e AH H O (9) 中的质量传输现象可分为 3 种形式:由浓度梯度引
3 2 起的扩散;由电场电势梯度引起的迁移;由溶液压
AH H O e A H O H (10)
3 2 2 力不平衡引起的对流。
2AH 2A H (11) 在理论上可以由 Nernst-Planck 方程描述,式
2
式中:A 为活性位点;AH 为 HER 中涉及的表面态。 (16)为 x 方向上的描述:
OER 中的 CPET 更为复杂,涉及 4 种表面态: J i ()x D c i i ()/x x ( F /R )z D i T ()/x x c v i ( )x (16)
i
2
A、AOH、AO、AOOH,基本步骤如式(12)~(15) 式中:J 为传质通量,mol/(m ·s);i 代表物质种类;
2
所示: D 为扩散系数,m /s;c 为浓度,mol/L;z 为电荷数;
AOH AOH e (12) F 为法拉第常数,96500 C/mol;R 为理想气体常数,
8.314 J/(mol·K);T 为温度,K;φ 为电势,V;v 为
AOHOH AOH O e
2 (13) 溶液流速,m/s。方程右边的第一项、第二项和第三
AO OH AOOH e (14) 项分别代表扩散、迁移和对流。
AOOH OH A O H O e
2 2 (15)
电解液中的离子成分通过直接参与表面质子化/
去质子化反应、或者改变局部 pH 间接影响反应物
和活性位点的方式影响质子电子转移过程。首先,
质子化/去质子化反应涉及纯化学反应,离子也可能
直接参与反应,在这个过程中,如磷酸盐、碳酸盐
等阴离子可能改变反应时的过渡态;而阳离子也会
通过影响 O—H 键的解离,进而影响到反应物浓度。 图 2 近电极表面的 3 种质量输运方式
+
–
另外,H 3 O 和 OH 作为水分解的反应物,在反应过 Fig. 2 Three modes of mass transfer close to the electrode
surface
程中的产生和消耗将导致电极附近的局部 pH 与体
相溶液中的 pH 产生较大差异,改变电极表面动力 其中扩散项(即 Fick 定律)通常可以与 Nernst 型
学的同时增大了溶液中的浓度梯度,而由离子带来 扩散模型结合使用,由此扩散通量可以表示为式(17):
/ c δ
的缓冲作用有助于维持局部的 pH,进而影响反应活 J diff D ( / )(D δ c c ) (17)
b s
性。最后,反应过程中,阴离子在一定条件下发生 式中:J diff 为扩散通量,mol/(m ·s);δ 为扩散层的厚
2
特异性吸附,阳离子也可以通过非共价作用或特异 度,m;下标 b 和 s 分别代表体相溶液和电极表面。
性吸附在表面产生阻塞,此时动力学也会因为反应 式(16)的第二项迁移是由带电物质的漂移引
活性位点数量的变化而改变,影响表面反应的发生。 起的,可用式(18)表示:
J migra uc / x (18)
i
2
式中:J migra 为迁移通量,mol/(m ·s);u 为离子迁移
2
率,m /(V·s),可由式(19)表示为:
u ||F /Rz D T (19)
由此可见,扩散和迁移均主要由扩散系数确定,
根据 Stokes-Einstein 方程,得到由式(20)描述的
扩散系数:
D k/3πT dμ (20)
式中:k 为 Boltzmann 常数,1.380649×10 –23 J/K;d
图 1 质子耦合电子转移示意图 [36]
Fig. 1 Schematic diagram of proton coupled electron 为水合形式的离子的有效直径(即 Stokes 直径),m;
transfer [36] μ 为溶液的黏度,Pa·s。总的来说,一般考虑离子有