Page 136 - 《精细化工》2022年第6期
P. 136
·1202· 精细化工 FINE CHEMICALS 第 39 卷
峰,在脱附过程中可以在温度较低(<400 ℃)时检
测到信号,推测是由于 Mn 1 Co 1 O x 吸附氧较早脱除出
来,这意味着更多的氧气可以很容易地从催化剂表
面释放出来。随着温度的升高,当温度大于 400 ℃
时,催化剂的晶格氧逐渐转移释放出来,Mn 1 Co 1 O x
在高温段出峰仍然较早,这说明 Mn 1 Co 1 O x 催化剂具
有较好的氧移动性。
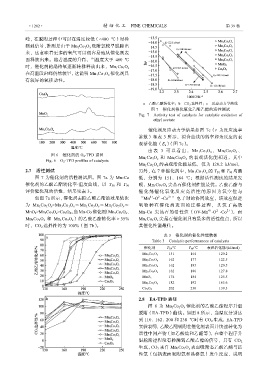
a—乙酸乙酯转化率;b—CO 2 选择性;c—反应动力学曲线
图 7 催化剂催化氧化乙酸乙酯的活性测试
Fig. 7 Activity test of catalysts for catalytic oxidation of
ethyl acetate
催化剂反应动力学结果如图 7c(r 为反应速率
常数)和表 3 所示,拟合曲线的斜率即为反应的表
观活化能(E a )(图 7c)。
由表 3 可以看出 ,Mn 1 Co 1 O x 、Mn 3 Co 1 O x 、
图 6 催化剂的 O 2 -TPD 谱图 Mn 1 Co 3 O x 和 Mn 1 Co 5 O x 的表观活化能相近,其中
Fig. 6 O 2 -TPD profiles of catalysts
Mn 1 Co 1 O x 的表观活化能最低,仅为 120.2 kJ/mol,
2.7 活性测试 另外,在 7 种催化剂中,Mn 1 Co 1 O x 的 T 50 和 T 90 均最
图 7 为催化剂的活性测试图。图 7a 为 Mn-Co 低,分别为 151、164 ℃;根据活性测试的结果发
催化剂的乙酸乙酯转化率-温度曲线,以 T 50 和 T 90 现,Mn 1 Co 1 O x 尖晶石催化剂性能最优。乙酸乙酯与
评价催化剂的活性,结果见表 3。 催化剂催化氧化反应高活性的原因为氧空位与
2+
2−
4+
如图 7a 所示,催化剂去除乙酸乙酯的效果依次 “Mn -O -Co ”电子对的协同效应,该效应促进
为 Mn 1 Co 1 O x >Mn 3 Co 1 O x ≈Mn 1 Co 3 O x ≈Mn 1 Co 5 O x ≈ 氧物种在催化剂表面的迁移过程,共筑了高效
2+
2−
4+
MnO 2 >Mn 5Co 1O x >Co 3 O 4。当 Mn-Co 催化剂(Mn 1Co 1 O x、 Mn-Co 尖晶石的活性位(OV-Mn -O -Co ),而
Mn 3 Co 1 O x 和 Mn 1 Co 3 O x )的乙酸乙酯转化率>35% Mn 1 Co 1 O x 尖晶石催化剂具有最多的活性位点,所以
时,CO 2 选择性约为 100%(图 7b)。 其催化性能最佳。
表 3 催化剂的催化性能数据
Table 3 Catalytic performances of catalysts
催化剂 T 50/℃ T 90/℃ 表观活化能/(kJ/mol)
Mn 1Co 1O x 151 164 120.2
162 177 122.5
Mn 3Co 1O x
162 185 120.5
Mn 1Co 5O x
162 186 127.8
Mn 1Co 3O x
MnO 2 174 184 125.5
182 192 165.6
Mn 5Co 1O x
202 230 139.3
Co 3O 4
2.8 EA-TPD 表征
图 8 为 Mn 1 Co 1 O x 催化剂的乙酸乙酯程序升温
脱附(EA-TPD)曲线。如图 8 所示,当温度分别达
到 110、162、200 和 238 ℃时有 CO 2 生成,EA-TPD
实验表明,乙酸乙酯吸附在催化剂表面并快速转化为
活性中间产物(如乙酸盐和乙醛等),在整个程序升
温脱附过程没有检测到乙酸乙酯的信号,只有 CO 2
生成,CO 2 来自 Mn 1 Co 1 O x 表面吸附态乙酸乙酯与活
性氧(包括表面吸附氧和晶格氧)发生反应,说明