Page 152 - 《精细化工》2021年第7期
P. 152
·1434· 精细化工 FINE CHEMICALS 第 38 卷
MPDA 粒子的电势为(–33.4±0.6) mV,经电势为
(13.3±0.2) mV 的 DOX 的负载,DOX@MPDA 纳米粒
子的电势为(–21.9±0.5) mV。电势的明显变化表明
DOX 成功负载到 MPDA 上,包裹 PLTM 后,电势
明显减小,进一步表明纳米药物传递系统成功制备。
2.2 载药率、包封率及药物释放情况
将载药实验得到的上清液中 DOX 的吸光度值
带入到之前绘制的 DOX 标准曲线中,并根据式(1)
和(2)计算得出载药率为 38.63%,包封率为 98.86%。
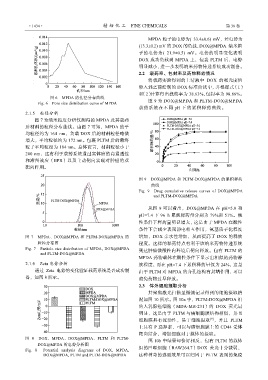
图 6 MPDA 的孔径分布曲线
Fig. 6 Pore size distribution curve of MPDA 图 9 为 DOX@MPDA 和 PLTM-DOX@MPDA
载药系统在不同 pH 下的累积释药曲线。
2.1.5 粒径分析
图 7 为纳米粒度分析仪测得的 MPDA 及其载药
后材料的粒径分布曲线。由图 7 可知,MPDA 的平
均粒径约为 164 nm,负载 DOX 后的材料粒径略微
增大,平均粒径约为 172 nm。包裹 PLTM 后的最终
粒子平均粒径为 184 nm。总体而言,材料粒径小于
200 nm,这有利于载药系统通过实体瘤的高通透性
和滞留效应(EPR)以及主动靶向实现对肿瘤的双
靶向作用。
图 9 DOX@MPDA 和 PLTM-DOX@MPDA 的累积释药
曲线
Fig. 9 Drug cumulative release curves of DOX@MPDA
and PLTM-DOX@MPDA
从图 9 可以看出,DOX@MPDA 在 pH=5.0 和
pH=7.4 下 96 h 累积释药量分别为 79%和 51%。酸
性条件下释药量明显增大,这是由于 MPDA 在酸性
条件下会减少表面静电相互作用,氨基质子化程度
图 7 MPDA、DOX@MPDA 和 PLTM-DOX@MPDA 的 增加,DOX 亲水性增加,从而提高了 DOX 的释放
粒径分布图 程度。这样的释药特点有利于该纳米药物传递系统
Fig. 7 Particle size distribution of MPDA, DOX@MPDA 到达肿瘤微酸性内环境后靶向释放。包有 PLTM 的
and PLTM-DOX@MPDA
MPDA 药物载体在酸性条件下显示出相似的药物释
2.1.6 Zeta 电势分析 放程度,而在 pH=7.4 下累积释药量仅为 24%,这是
通过 Zeta 电势的变化验证载药系统是否成功制 由于 PLTM 对 MPDA 的介孔结构有封堵作用,可以
备,如图 8 所示。 避免药物过早释放。
2.3 体外细胞摄取分析
共聚焦激光扫描显微镜记录得到的细胞摄取情
况如图 10 所示。图 10a 中,PLTM-DOX@MPDA 组
的人乳腺癌细胞(MDA-MB-231)的 DOX 荧光最
明显,这是由于 PLTM 与癌细胞膜结构相似,并且
[9]
细胞膜具有流动性,易于细胞摄取 ,并且 PLTM
上具有 P 选择素,可以与癌细胞膜上的 CD44 受体
靶向结合,增加细胞对于载体的摄取。
图 8 DOX、MPDA、DOX@MPDA、PLTM 和 PLTM- 图 10b 中结果却恰好相反,包有 PLTM 的载体
DOX@MPDA 的电势分析图
Fig. 8 Potential analysis diagrams of DOX, MPDA, 组的巨噬细胞(RAW264.7)DOX 荧光十分微弱,
DOX@MPDA, PLTM and PLTM-DOX@MPDA 这种神奇的逃避效果可以归因于 PLTM 表面的免疫